题目内容
9.水溶液X中只可能溶有Na+、Ca2+、Fe3+、[Al(OH)4]-、SiO32-、CO32-、SO42-中的若干种离子.某同学对该溶液迸行了如下实验:下列判断正确的是( )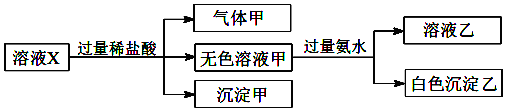
| A. | 气体甲一定是纯净物 | |
| B. | 沉淀甲是硅酸和硅酸钙的混合物 | |
| C. | CO32-和SO42-一定不存在于溶液X中 | |
| D. | Na+、[Al(OH)4]-和SiO32-一定存在于溶液X中 |
分析 X中只可能溶有Na+、Ca2+、Fe3+、[Al(OH)4]-、SiO32-、CO32-、SO42-中的若干种离子,由实验可知沉淀甲为H2SiO3,气体甲含CO2,因盐酸易挥发,甲中可能混有HCl,则原溶液中一定含SiO32-、CO32-,则不含Ca2+、Fe3+,由溶液甲与氨水反应生成白色沉淀乙为Al(OH)3,溶液乙含氯化铵,则原溶液一定含[Al(OH)4]-,由电荷守恒可知,溶液含阳离子为Na+,不能确定是否含SO42-,以此来解答.
解答 解:A.由上述分析可知,甲可能为CO2、HCl的混合物,故A错误;
B.沉淀甲是硅酸沉淀,由离子共存可知原溶液中不含Ca2+,故B错误;
C.不能确定是否含SO42-,故C错误;
D.由上述分析可知,Na+、[Al(OH)4]-和SiO32-一定存在于溶液X中,故D正确;
故选D.
点评 本题考查常见离子的检验,为高频考点,把握流程中发生的反应、离子检验方法、离子共存为解答的关键,侧重分析与应用能力的考查,注意气体及沉淀的判断,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
4.“84消毒液”因1984年北京某医院研制使用而得名,在日常生活中使用广泛,其有效成分是NaClO.某小组在实验室制备NaClO溶液,并进行性质探究和成分测定.

(1)该小组按上图装置进行实验,反应一段时间后,分别取B、C、D瓶的溶液进行实验,实验现象如表.(已知饱和NaClO溶液pH为11)
①装置A中反应的化学方程式为KClO3+6HCl=3Cl2↑+KCl+3H2O.
②B瓶溶液中H+的主要来源是氯气中混有氯化氢.
③C瓶溶液的溶质是NaClO、NaCl、NaOH(填化学式).
④结合平衡移动原理解释D瓶溶液中石蕊立即褪色的原因溶液中存在平衡Cl2+H2O?HCl+HClO,HCO3-消耗H+,使平衡右移,HClO浓度增大.
(2)测定C瓶溶液中NaClO含量(单位:g•L-1)的实验步骤如下:
Ⅰ.取C瓶溶液20mL于锥形瓶,加足量盐酸酸化,迅速加入过量KI溶液,盖紧瓶塞并在暗处充分反应.
Ⅱ.用0.1000mol•L-1Na2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点时共用去20.00mL Na2S2O3溶液.(I2+2S2O32-═2I-+S4O62-)
①NaClO的电子式为 .
.
②步骤Ⅰ总反应的离子方程式为ClO-+2I-+2H+=I2+Cl-+H2O.
③C瓶溶液中NaClO的含量为3.7g•L-1.(保留1位小数.NaClO式量为74.5)

(1)该小组按上图装置进行实验,反应一段时间后,分别取B、C、D瓶的溶液进行实验,实验现象如表.(已知饱和NaClO溶液pH为11)
| 实验步骤 | 实验现象 | ||
| B瓶 | C瓶 | D瓶 | |
| 实验1:取样,滴加紫色石蕊溶液 | 变红,缓慢褪色 | 变红,缓慢褪色 | 立即褪色 |
| 实验2:取样,测定溶液的pH | 3 | 12 | 7 |
②B瓶溶液中H+的主要来源是氯气中混有氯化氢.
③C瓶溶液的溶质是NaClO、NaCl、NaOH(填化学式).
④结合平衡移动原理解释D瓶溶液中石蕊立即褪色的原因溶液中存在平衡Cl2+H2O?HCl+HClO,HCO3-消耗H+,使平衡右移,HClO浓度增大.
(2)测定C瓶溶液中NaClO含量(单位:g•L-1)的实验步骤如下:
Ⅰ.取C瓶溶液20mL于锥形瓶,加足量盐酸酸化,迅速加入过量KI溶液,盖紧瓶塞并在暗处充分反应.
Ⅱ.用0.1000mol•L-1Na2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点时共用去20.00mL Na2S2O3溶液.(I2+2S2O32-═2I-+S4O62-)
①NaClO的电子式为
 .
.②步骤Ⅰ总反应的离子方程式为ClO-+2I-+2H+=I2+Cl-+H2O.
③C瓶溶液中NaClO的含量为3.7g•L-1.(保留1位小数.NaClO式量为74.5)
20.工业上制备粗硅的反应为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,下列说法正确的是( )
| A. | SiO2是还原剂 | B. | C被氧化 | ||
| C. | SiO2发生氧化反应 | D. | C得到电子 |
17.在甲、乙两个密闭容器中.分别充有质量相同的O2、H2两种气体,若两容器温度和密度均相同,则下列说法正确的是( )
| A. | 甲的体积比乙的体积大 | B. | 甲的分子数比乙的分子致少 | ||
| C. | 甲的压强比乙的压强大 | D. | 甲的摩尔体积比乙的华尔体积大 |
14.将3mol•L-1的Ca(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为( )
| A. | $\frac{6a}{b}$ mol•L-1 | B. | $\frac{3a}{b}$ mol•L-1 | C. | $\frac{3b}{a}$ mol•L-1 | D. | $\frac{b}{a}$ mol•L-1 |
19.下列各装置不能构成原电池的是(电解质溶液均为稀硫酸)( )
| A. |  | B. | 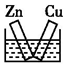 | C. | 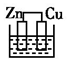 | D. |  |
