题目内容
18.由于A2+3B2═2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )| A. | v(B2)=0.8 mol•L-1•s-1 | B. | v(A2)=0.4 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(B2)=0.42 mol•L-1•s-1 |
分析 由于不同物质表示的速率之比等于化学计量数之比,故不同物质质表示的反应速率与其化学计量数的比值越大,则表示的反应速率越快.
解答 解:对于反应A2+3B2?2C,都转化为B2表示的速率进行比较:
A.v(B2)=0.8 mol•L-1•s-1;
B.v(B2)=3v(A2)=3×0.4 mol•L-1•s-1=1.2mol•L-1•s-1;
C.v(B2)=$\frac{3}{2}$v(C)=$\frac{3}{2}$×0.6mol•L-1•s-1=0.9mol•L-1•s-1;
D.v(B2)=0.42 mol•L-1•s-1;
故B选项中表示的反应速率最快,
故选B.
点评 本题考查反应速率的比较,注意转化为同种物质的反应速率来比较,也可以利用反应速率与化学计量数的比值进行判断,比值越大,反应速率越快,难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
8.一种一元强酸HA溶液中加入一种碱MOH反应后,溶液呈中性,下列判断中正确的是( )
| A. | 若为强碱,则需加入的碱过量 | |
| B. | 混合前酸与碱中溶质的物质的量相等 | |
| C. | 生成的盐不发生水解 | |
| D. | 反应溶液中c(A-)、c(M+)相等 |
9.下列表述正确的是( )
| A. | c(OH-)/c(H+)═10-12的溶液中:NH4+、Cu2+、NO3-、Cl-能大量共存 | |
| B. | 通入过量SO2气体的溶液中:HSO3-、NO3-、Ba2+不能大量共存 | |
| C. | 向足量NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液的离子方程式为:HCO3-+Ba2++H++SO42-═BaSO4↓+H2O+CO2↑ | |
| D. | 向Fe(NO3)3溶液中加入HI溶液的离子方程式为:2Fe3++2I-═2Fe2++2I2 |
3.将自来水管与下列材料做成的水龙头连接,使铁水管锈蚀最快的水龙头是( )
| A. | 塑料水龙头 | B. | 陶瓷水龙头 | C. | 铜水龙头 | D. | 铁水龙头 |
7.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是Ar(填具体元素符号,下同),原子结构示意图为 ;元素⑩名称为Br.
;元素⑩名称为Br.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是: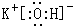 .
.
(3)元素⑤与⑦形成化合物的化学式为AlCl3;实验测得,当此化合物在液态或固态时不导电,溶解于水时能导电,由此判断该化合物属于共价化合物.
(4)元素③、⑥、⑦形成的气态氢化物中,沸点最高的物质的化学式是H2O,原因是H2O分子间含有氢键.
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 ;元素⑩名称为Br.
;元素⑩名称为Br.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是:
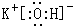 .
.(3)元素⑤与⑦形成化合物的化学式为AlCl3;实验测得,当此化合物在液态或固态时不导电,溶解于水时能导电,由此判断该化合物属于共价化合物.
(4)元素③、⑥、⑦形成的气态氢化物中,沸点最高的物质的化学式是H2O,原因是H2O分子间含有氢键.
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
8.已知还原性I->Fe2+>Br-,下列离子方程式正确的是( )
| A. | 将少量Cl2通入FeBr2溶液中:Cl2+2Br-═Br2+2Cl- | |
| B. | 将足量Cl2通入FeBr2溶液中:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| C. | 将少量Cl2通入FeI2溶液中:2Fe2++2I-+3Cl2═2Fe3++2I2+6Cl- | |
| D. | 将672mLCl2(标况)通入250mL 0.1molL-1的FeI2溶液中:2Fe2++10I-+6Cl2═12Cl-+5I2+2Fe3+ |
 ,C
,C .
.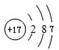 ,D微粒的结构示意图是
,D微粒的结构示意图是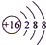 ,写出E的三种核素11H、21H、31H.
,写出E的三种核素11H、21H、31H.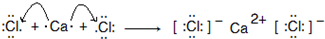 .
.