题目内容
3.将自来水管与下列材料做成的水龙头连接,使铁水管锈蚀最快的水龙头是( )| A. | 塑料水龙头 | B. | 陶瓷水龙头 | C. | 铜水龙头 | D. | 铁水龙头 |
分析 根据要使铁水管锈蚀最快,则应形成原电池,且在形成的原电池中,铁水管应做负极,从而能加快铁水管的腐蚀,据此分析.
解答 解:A、将塑料水龙头和铁水管相连不能形成原电池,腐蚀教慢;
B、陶瓷不能导电,故将铁水管和陶瓷水龙头相连,不能形成原电池,铁水管的腐蚀不能被加快;
C、将铁水管和铜水龙头相连,铜水龙头做正极,铁水管做负极,铁水管的腐蚀被加快;
D、将铁水管和铁水龙头相连,不能形成原电池,故不能加快反应速率,腐蚀不能被加快.
综上比较,使铁水管腐蚀最快的是铜水龙头,故选C.
点评 本题考查了金属锈蚀的条件,完成此题,依据与水龙头材料要形成原电池才符合题意.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
13.下列离子能大量共在的是( )
| A. | Ba2+、Na+、OH-、SO42- | B. | H+、Na+、I-、Cl- | ||
| C. | HCO3-、K+、NO3-、OH- | D. | H+、Fe2+、SO42-、NO3- |
14.下列解释亊实的离子方程式不正碥的是( )
| A. | 用Na2S去除废水中的Hg2+,Hg2++S2-═HgS↓ | |
| B. | 向Fe(NO3)2溶液中滴人稀硫酸.溶液由浅绿色变为黄色3Fe2++4H++NO3-=3Fe2++NO↑+2H2O | |
| C. | 用醋酸、淀粉碘化钾试纸检测加碘食盐中是否有KIO3,IO3-+6I-+6H+=3I2+3H2O | |
| D. | 消毒液的主要成分为NaClO溶液,与洁厨灵混用.产生有毐Cl2,2H+++Cl-+ClO-=Cl2↑+H2O |
18.由于A2+3B2═2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
| A. | v(B2)=0.8 mol•L-1•s-1 | B. | v(A2)=0.4 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(B2)=0.42 mol•L-1•s-1 |
8.图为元素周期表中短周期的一部分, 四种元素中只有一种是金属,下列说法错误的是( )
四种元素中只有一种是金属,下列说法错误的是( )
 四种元素中只有一种是金属,下列说法错误的是( )
四种元素中只有一种是金属,下列说法错误的是( )| A. | 气态氢化物稳定性:R>Q | |
| B. | 元素T的离子结构示意图为 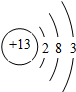 | |
| C. | 与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键 | |
| D. | Q的一种同位素可用于测定文物的年代 |
15.保护环境,就是关爱自己.下列说法中你认为不正确的是( )
| A. | 空气质量日报的主要目的是树立人们环保意识,同时也让人们知道了二氧化硫、二氧化氮和可吸入颗粒物是大气主要污染物 | |
| B. | 酸雨是指pH小于7的雨水 | |
| C. | 为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须进行回收处理 | |
| D. | 食品厂产生的含丰富氮、磷营养素的废水不可以长期排向水库 |
12.下列关于物质性质变化的比较,不正确的是( )
| A. | 稳定性:HI>HBr>HCl>HF | B. | 原子半径大小:Na>S>O | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 还原性强弱:Cl-<Br-<I- |
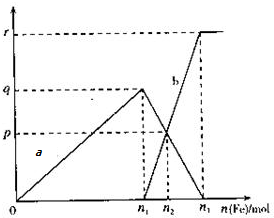 在11.2mol/L的稀硝酸溶液中逐渐加入铁粉,反应中氧化产物的物质的量与加入的铁粉的物质的量的关系如图所示(其中纵坐标为氧化产物的物质的量,横坐标为加入铁粉的物质的量),请回答以下问题:
在11.2mol/L的稀硝酸溶液中逐渐加入铁粉,反应中氧化产物的物质的量与加入的铁粉的物质的量的关系如图所示(其中纵坐标为氧化产物的物质的量,横坐标为加入铁粉的物质的量),请回答以下问题: