题目内容
9.下列表述正确的是( )| A. | c(OH-)/c(H+)═10-12的溶液中:NH4+、Cu2+、NO3-、Cl-能大量共存 | |
| B. | 通入过量SO2气体的溶液中:HSO3-、NO3-、Ba2+不能大量共存 | |
| C. | 向足量NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液的离子方程式为:HCO3-+Ba2++H++SO42-═BaSO4↓+H2O+CO2↑ | |
| D. | 向Fe(NO3)3溶液中加入HI溶液的离子方程式为:2Fe3++2I-═2Fe2++2I2 |
分析 A.该溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应;
B.硝酸根离子在酸性条件下能够氧化亚硫酸氢根离子、二氧化硫;
C.硫酸氢钠足量,离子方程式按照碳酸氢钡的化学式书写;
D.硝酸根离子在酸性条件下具有强氧化性,优先氧化碘离子.
解答 解:A.c(OH-)/c(H+)═10-12的溶液呈酸性,溶液中存在大量氢离子,NH4+、Cu2+、NO3-、Cl-之间不反应,都不与氢离子反应,能够大量共存,故A正确;
B.通入二氧化硫气体后溶液呈酸性,HSO3-、NO3-之间发生氧化还原反应,在溶液中不能大量共存,故B错误;
C.向足量NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液,钡离子与碳酸氢根离子的物质的量之比为1:2,正确的离子方程式为:2HCO3-+Ba2++2H++SO42-═BaSO4↓+2H2O+2CO2↑,故C错误;
D.硝酸的氧化性大于铁离子,若HI足量,硝酸根离子和铁离子都完全反应,正确的离子方程式为:10I-+3NO3-+Fe3++12H+═5I2+3NO↑+Fe2++6H2O,故D错误;
故选A.
点评 本题考查离子共存的正误判断、离子方程式的书写,为高考的高频题,属于中等难度的试题,注意掌握离子方程式书写原则,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
19.科学家发现了一种新元素的原子核内有161个中子,质量数为272,该元素的核电荷数为( )
| A. | 111 | B. | 161 | C. | 272 | D. | 433 |
20.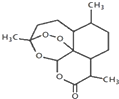 我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法合理的是( )
我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法合理的是( )
 我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法合理的是( )
我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法合理的是( )| A. | 化学式为C15H20O5 | |
| B. | 只含有氧原子一种官能团 | |
| C. | 能发生取代反应和氧化反应 | |
| D. | 可用乙醇从青蒿浸取液中萃取出青蒿素 |
17.分离提纯是化工生产中常用的方法.下列说法合理的是( )
| A. | 蒸馏自来水可得到蒸馏水 | B. | 酸溶法除去Al2O3的Fe2O3 | ||
| C. | 过滤法除去乙酸中的乙醇 | D. | 碱溶法除去Al2O3中的SiO2 |
4.下列有关说法正确的是( )
| A. | 反应时构成分子的原子种类发生改变 | |
| B. | 分子、原子、离子都是构成物质的微粒 | |
| C. | 不同元素最本质的区别在是相对原子质量不同 | |
| D. | 原子不显电性,是因为原子中不存在带电的粒子 |
14.下列解释亊实的离子方程式不正碥的是( )
| A. | 用Na2S去除废水中的Hg2+,Hg2++S2-═HgS↓ | |
| B. | 向Fe(NO3)2溶液中滴人稀硫酸.溶液由浅绿色变为黄色3Fe2++4H++NO3-=3Fe2++NO↑+2H2O | |
| C. | 用醋酸、淀粉碘化钾试纸检测加碘食盐中是否有KIO3,IO3-+6I-+6H+=3I2+3H2O | |
| D. | 消毒液的主要成分为NaClO溶液,与洁厨灵混用.产生有毐Cl2,2H+++Cl-+ClO-=Cl2↑+H2O |
1.下列化学式与指定物质的主要成分对应正确的是( )
| A. | 光导纤维--Si | B. | 熟石灰--CaO | ||
| C. | 水煤气--CO、H2 | D. | 绿矾--Fe2(SO4)3•7H2O |
18.由于A2+3B2═2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
| A. | v(B2)=0.8 mol•L-1•s-1 | B. | v(A2)=0.4 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(B2)=0.42 mol•L-1•s-1 |