题目内容
13.有A、B、C、D、E五种单核微粒:①当A微粒失去3个电子后,电子层结构与氖原子的相同;②B微粒得到一个电子后,其电子层结构与氩原子相同;③C微粒是带两个单位正电荷,核电荷数为12的阳离子;④D微粒18个电子,带两个单位的负电荷;⑤E微粒不带电,原子核中只有一个质子.请回答:(1)写出各微粒的符号:AAl、BCl、CMg2+、DS2-、EH.
(2)B微粒的结构示意图是
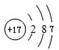 ,D微粒的结构示意图是
,D微粒的结构示意图是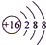 ,写出E的三种核素11H、21H、31H.
,写出E的三种核素11H、21H、31H.
分析 有A、B、C、D、E五种单核微粒:
①当A微粒失去3个电子后,电子层结构与氖原子的相同,则A为Al;
②B微粒得到一个电子后,其电子层结构与氩原子相同,则B为Cl;
③C微粒是带两个单位正电荷,核电荷数为12的阳离子,则C为Mg2+;
④D微粒18个电子,带两个单位的负电荷,则D为S2-;
⑤E微粒不带电,原子核中只有一个质子,则E为H原子.
解答 解:(1)有A、B、C、D、E五种单核微粒:
①当A微粒失去3个电子后,电子层结构与氖原子的相同,则A为Al;
②B微粒得到一个电子后,其电子层结构与氩原子相同,则B为Cl;
③C微粒是带两个单位正电荷,核电荷数为12的阳离子,则C为Mg2+;
④D微粒18个电子,带两个单位的负电荷,则D为S2-;
⑤E微粒不带电,原子核中只有一个质子,则E为H原子,
故答案为:Al;Cl;Mg2+;S2-;H;
(2)B微粒的结构示意图是 ,D微粒的结构示意图是
,D微粒的结构示意图是 ,E的三种核素为11H、21H、31H,
,E的三种核素为11H、21H、31H,
故答案为: ;
; ;11H、21H、31H.
;11H、21H、31H.
点评 本题考查了原子核外电子排布及质子数、中子数、质量数的相互关系等知识点,侧重考查学生对基础知识的掌握.

练习册系列答案
相关题目
3.将1mol乙醇(其中的氧用18O标记)在浓硫酸存在条件下与足量乙酸充分反应.下列叙述不正确的是( )
| A. | 生成的乙酸乙酯中含有18O | B. | 生成的水分子中不含18O | ||
| C. | 可能生成44g乙酸乙酯 | D. | 可能生成90g乙酸乙酯 |
4.下列有关说法正确的是( )
| A. | 反应时构成分子的原子种类发生改变 | |
| B. | 分子、原子、离子都是构成物质的微粒 | |
| C. | 不同元素最本质的区别在是相对原子质量不同 | |
| D. | 原子不显电性,是因为原子中不存在带电的粒子 |
1.下列化学式与指定物质的主要成分对应正确的是( )
| A. | 光导纤维--Si | B. | 熟石灰--CaO | ||
| C. | 水煤气--CO、H2 | D. | 绿矾--Fe2(SO4)3•7H2O |
18.由于A2+3B2═2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
| A. | v(B2)=0.8 mol•L-1•s-1 | B. | v(A2)=0.4 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(B2)=0.42 mol•L-1•s-1 |
5.用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L的FeCl2溶液,研究废液再生机理.记录如下(a、b、c代表电压数值):
(1)用FeCl3酸性溶液脱除H2S的离子方程式为2Fe3++H2S═S↓+2Fe2++2H+
(2)用KSCN检验出Fe3+的离子方程式为Fe3++3SCN-═Fe(SCN)3.
(3)Ⅰ中,Fe3+产生的原因可能是:Cl-在阳极放电(或Cl-失电子生成Cl2),生成的Cl2将Fe2+氧化.
(4)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(5)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
①NaCl的浓度是0.2mol/L
②Ⅳ中检测Cl2的实验方法湿润的淀粉碘化钾检验生成气体,试纸变蓝.
③与Ⅱ对比,得出的结论(写出两点):通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)用KSCN检验出Fe3+的离子方程式为Fe3++3SCN-═Fe(SCN)3.
(3)Ⅰ中,Fe3+产生的原因可能是:Cl-在阳极放电(或Cl-失电子生成Cl2),生成的Cl2将Fe2+氧化.
(4)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(5)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
②Ⅳ中检测Cl2的实验方法湿润的淀粉碘化钾检验生成气体,试纸变蓝.
③与Ⅱ对比,得出的结论(写出两点):通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
2.已知:已知:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-25kJ/mol,某温度下的平衡常数为400.此温度下,在1L的密闭容器中加入CH3OH,反应到不同时刻测得各组分的物质的量浓度如下表,下列说法正确的是( )
| 物质 | CH3OH | CH3OCH3 | H2O |
| t1 | 0.8 | 1.24 | 1.24 |
| t2 | 0.08 | 1.6 | 1.6 |
| A. | 平衡后升高温度,平衡常数>400 | |
| B. | t2时刻反应达到平衡状态 | |
| C. | 平衡时,反应混合物的总能量减少20kJ | |
| D. | 平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大 |
3.下列有机物中,能在一定条件下发生消去反应且生成的烯烃只有一种的是( )
| A. | 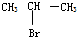 | B. | 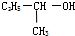 | C. | CH3OH | D. | 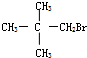 |