题目内容
10.《自然》杂志报道了我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”.完成下列填空:(1)10Be和9BeCD.
A.是同一种原子 B.具有相同的中子数
C.具有相同的化学性质 D.自然界中具有恒定的含量
(2)根据对角线原则,Be和Al的化学性质相似,请写出Be与NaOH溶液反应生成Na2BeO2的化学反应方程式:Be+2NaOH=Na2BeO2+H2↑.
(3)研究表明26Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是BC.
A.比较这两种元素的单质的硬度和熔点
B.将打磨过的镁带和铝片分别和同浓度同体积的盐酸反应
C.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液
D.将空气中放置已久的这两种元素的单质分别和热水作用
(4)目前还有一种测量方法叫“钾氩测年法”.写出两种和Ar核外电子排布相同的阴离子S2-、Cl-(用化学
符号表示);其中一种离子与钾相邻元素的离子所形成的化合物可用做干燥剂,用电子式表示该化合物的形成过程
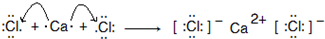 .
.
分析 (1)中子数不同质子数相同的原子为同种元素的不同核素互为同位素,同位素的化学性质是相似;
(2)金属铝和强碱反应产物是盐和氢气,所以Be与氢氧化钠溶液反应的产物是一种盐和氢气;
(3)比较元素的金属性强弱,可根据金属与水、酸反应的剧烈程度、对应的最高价氧化物的水化物的碱性强弱、单质间的置换反应等判断,以此解答该题;
(4)Ar具有18个电子,与Ar同周期的非金属元素得电子后与Ar电子数相同;根据电子式的书写方法来书写即可.
解答 解:(1)10Be和9Be是中子数不同、质子数相同的Be原子,互为同位素,它们的化学性质相似;
故答案为:CD;
(2)金属铍和氢氧化钠反应的化学方程式为:Be+2NaOH═Na2BeO2+H2↑,
故答案为:Be+2NaOH═Na2BeO2+H2↑;
(3)A.硬度和熔点属于物理性质,不能用于比较金属性,故A错误;
B.将打磨过的镁带和铝片分别和同浓度同体积的盐酸反应,Mg与HCl反应比Al与盐酸反应更剧烈,说明Mg比Al活泼,能证明金属性强弱,故B正确;
C、将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液,发现放镁带的那个变红色,证明金属镁可以和热水反应,但是金属铝不可以,能证明金属性强弱,故C正确;
D.将空气中久置的镁带和铝片分别置于热水中,由于二者表面有氧化膜,所以不与水反应,均无现象,故D错误;
故答案为:BC;
(4)Ar具有18个电子,与Ar同周期的非金属元素得电子后与Ar电子数相同,Ar核外电子排布相同的简单阴离子是硫离子和氯离子;与钾相邻元素的离子是钙离子,氯化钙可以做干燥剂,属于离子化合物,电子式为: ,用电子式表示该化合物的形成过程为
,用电子式表示该化合物的形成过程为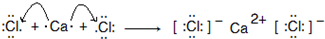 ;
;
故答案为:S2-、Cl-;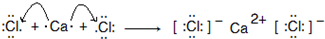 .
.
点评 本题涉及同位素的概念、元素金属性强弱的判断、微粒半径大小比较方法以及电子式的书写知识,属于综合知识的考查,难度中等,侧重于考查学生对基础知识的综合应用能力.

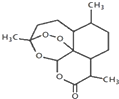 我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法合理的是( )
我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法合理的是( )| A. | 化学式为C15H20O5 | |
| B. | 只含有氧原子一种官能团 | |
| C. | 能发生取代反应和氧化反应 | |
| D. | 可用乙醇从青蒿浸取液中萃取出青蒿素 |
| A. | 光导纤维--Si | B. | 熟石灰--CaO | ||
| C. | 水煤气--CO、H2 | D. | 绿矾--Fe2(SO4)3•7H2O |
| A. | v(B2)=0.8 mol•L-1•s-1 | B. | v(A2)=0.4 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(B2)=0.42 mol•L-1•s-1 |
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)用KSCN检验出Fe3+的离子方程式为Fe3++3SCN-═Fe(SCN)3.
(3)Ⅰ中,Fe3+产生的原因可能是:Cl-在阳极放电(或Cl-失电子生成Cl2),生成的Cl2将Fe2+氧化.
(4)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(5)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
②Ⅳ中检测Cl2的实验方法湿润的淀粉碘化钾检验生成气体,试纸变蓝.
③与Ⅱ对比,得出的结论(写出两点):通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
| A. | 空气质量日报的主要目的是树立人们环保意识,同时也让人们知道了二氧化硫、二氧化氮和可吸入颗粒物是大气主要污染物 | |
| B. | 酸雨是指pH小于7的雨水 | |
| C. | 为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须进行回收处理 | |
| D. | 食品厂产生的含丰富氮、磷营养素的废水不可以长期排向水库 |
| 物质 | CH3OH | CH3OCH3 | H2O |
| t1 | 0.8 | 1.24 | 1.24 |
| t2 | 0.08 | 1.6 | 1.6 |
| A. | 平衡后升高温度,平衡常数>400 | |
| B. | t2时刻反应达到平衡状态 | |
| C. | 平衡时,反应混合物的总能量减少20kJ | |
| D. | 平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大 |
