题目内容
7.把0.6mol X气体和0.4mol Y气体混合于2L容器中,使它们发生如下反应:3X(g)+Y(g)?nZ(g)+2W(g),在5min时生成0.2mol W,若测知以Z的浓度变化表示反应速率为0.04mol•L-1•min-1,则上述反应中Z气体的化学计量数n的值是( )| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
分析 根据v=$\frac{△c}{△t}$计算v(W),再利用速率之比等于化学计量数之比计算n.
解答 解:在5min时生成0.2mol W,则v(W)=$\frac{\frac{0.2mol}{2L}}{5min}$=0.02mol•L-1•min-1,
率之比等于化学计量数之比,则v(W):v(Z)=2:n=0.02mol•L-1•min-1:0.04mol•L-1•min-1=1:2,故n=4,
故选:A.
点评 本题考查化学反应速率与化学计量数关系,比较基础,注意根据速率定义式理解,有利于基础知识的巩固.

练习册系列答案
相关题目
17.下列有关硅及其化合物的叙述中,错误的是( )
| A. | 单质硅是良好的半导体材料 | B. | 硅常温时可以和强碱反应 | ||
| C. | 二氧化硅广泛存在于自然界 | D. | 硅酸是挥发性酸 |
18.下列有关实验说法正确的是( )
| A. | 在“阿司匹林的合成”实验中,把从盐酸中析出的晶体进行抽滤,用乙醇洗涤晶体1~2次,然后抽滤,将晶体转移到表面皿上,干燥后称其质量,计算产率 | |
| B. | 制备摩尔盐时,最后在蒸发皿中蒸发浓缩溶液,加热至液体表面出现晶膜为止,不能溶液全部蒸干 | |
| C. | 晶体颗粒的大小与结晶条件有关,溶质的溶解度越小,或溶液的浓度越高,或溶剂的蒸发速度越快,析出的晶粒就越细大 | |
| D. | 在“食醋总酸含量测定”实验中,将食醋稀释10倍后再滴定是为了减少食醋的浪费 |
2.表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍.下列说法正确的是( )
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的气态氢化物的热稳定性均依次递增 | |
| B. | Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | YX2和WX3均属于离子化合物 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2Y3具有氧化性和还原性 |
12.用石墨作电极电解1mol•L-1下列物质的溶液,一段时间后溶液的pH增大的是( )
①H2SO4 ②NaOH ③Na2SO4 ④NaCl.
①H2SO4 ②NaOH ③Na2SO4 ④NaCl.
| A. | 只有① | B. | ②④ | C. | ①②④ | D. | ①②③④ |
19.少量铁粉与100mL 0.01mol•L-1的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法的( )
①加H2O
②滴入几滴浓HNO3
③滴入几滴浓盐酸
④加CH3COONa固体
⑤加NaCl固体
⑥升高温度(不考虑盐酸挥发)
⑦改用10mL 0.1mol•L-1盐酸.
①加H2O
②滴入几滴浓HNO3
③滴入几滴浓盐酸
④加CH3COONa固体
⑤加NaCl固体
⑥升高温度(不考虑盐酸挥发)
⑦改用10mL 0.1mol•L-1盐酸.
| A. | ②⑥⑦ | B. | ③⑤⑦ | C. | ③⑥⑦ | D. | ②③⑦ |
16.铜有两种常见的氧化物CuO和Cu2O.某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示.则下列分析正确的是( )
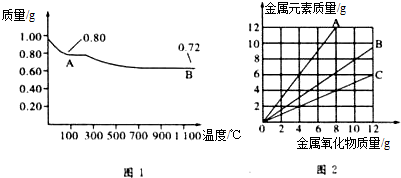

| A. | 图1中,A到B的过程中有0.005mol电子发生了转移 | |
| B. | 图1整个过程中共生成0.18g水 | |
| C. | 图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A | |
| D. | 图1中A和B化学式分别为Cu2O和CuO |
17.土卫六“泰坦”拥有丰富的碳氢燃料资源.“泰坦”的碳氢化合物循环在一定程度上与地球的水循环类似,以甲烷雨和碳氢雾的形式出现,或者以液态甲烷和乙烷湖的形式存在于地表,下列有关说法正确的是( )
| A. | 碳氢化合物就是烃 | |
| B. | 水、甲烷和乙烷都是10个电子的分子 | |
| C. | 乙烷的沸点比甲烷高,因而更难液化 | |
| D. | 甲烷和乙烷分子中只有一种氢,故其二氯化物也只有一种 |