题目内容
10.石油裂解产品A是衡量一个国家石油化工发展水平的标志.由A合成有机产品F的流程如下: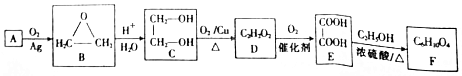
回答下列问题:
(1)A的名称是乙烯;C的官能团名称是羟基.
(2)F的结构简式为CH3CH2OOCCOOCH2CH3;由E生成F的反应类型是酯化反应.
(3)在一定条件下A可合成高分子化合物M,M常用作食品包装材料.写出由A合成M的化学方程式:nCH2═CH2$\stackrel{催化剂}{→}$
 .
.
分析 A是石油裂解主要产物之一,其产量可以用来衡量一个国家的石油化工水平,A为CH2=CH2,由流程图可知B为环氧乙烷、C为乙二醇、C催化氧化生成D,则D为OHCCHO、D催化氧化生成E,E为HOOCCOOH,E与乙醇发生酯化反应生成F,则F为CH3CH2OOCCOOCH2CH3,据此分析解答.
解答 解:(1)由上述分析可知,A的结构简式为CH2=CH2,名称是乙烯,C为乙二醇,官能团名称是羟基,故答案为:乙烯;羟基;
(2)由上述分析可知,F的结构简式为CH3CH2OOCCOOCH2CH3;E与乙醇发生酯化反应生成F,由E生成F的反应类型是酯化反应;
故答案为:CH3CH2OOCCOOCH2CH3;酯化反应;
(3)由上述分析可知,A的结构简式为CH2=CH2,可合成高分子化合物M为聚乙烯,则反应的化学方程式为nCH2═CH2$\stackrel{催化剂}{→}$ ,故答案为:nCH2═CH2$\stackrel{催化剂}{→}$
,故答案为:nCH2═CH2$\stackrel{催化剂}{→}$ .
.
点评 本题考查有机物推断、烯与醇、醛、羧酸之间的转化关系等,难度不大,注意基础知识的理解掌握.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
7.将铁屑溶于过量盐酸后,再加入下列物质:①稀硫酸;②硝酸钠;③氯化铜;④氯水,产生 Fe3+的是( )
| A. | ①④ | B. | ②④ | C. | 只有④ | D. | ①③ |
1.下列溶液中浓度关系正确的是( )
| A. | 小苏打溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | CH3COONa溶液中:c(CH3COO-)>c(Na+) | |
| C. | 物质的量浓度相等的CH3COOH溶液和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) | |
| D. | 常温下,0.1mol/L的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H2A)>c(A2-) |
5.某溶液中可能含有K+、SO32-、CO32-、SiO32-,向该溶液中加人稀盐酸,产生白色浑浊和无色无味气体,下列说法正确的是( )
| A. | 无法判断该溶液中是否含有K+ | |
| B. | 该溶液中一定含有K+、SiO32-,可能含有CO32- | |
| C. | 该溶液中无SO32-,一定含有CO32- | |
| D. | 该溶液中可能含有K+和CO32- |
15.下列物质的碱性及对应的解释均正确的是( )
| 选项 | 物质 | 酸碱性 | 解释 |
| A | K2CO3 | 碱性 | CO32-+2H2O═H2CO3+2OH- |
| B | NH4NO3 | 碱性 | NH4++H2O?NH3•H2O+H+ |
| C | Cu(ClO4)2 | 酸性 | Cu2++2H2O═Cu(OH)2↓+2H+ |
| D | NaHSO3 | 酸性 | HSO3-?H++SO32- |
| A. | A | B. | B | C. | C | D. | D |
2.把10.26g 由Na2CO3•10H2O和NaHCO3组成的固体混合物溶于水配成200mL溶液,其中c(Na+)=0.4mol•L-1.则原固体混合物中Na2CO3•10H2O和NaHCO3的物质的量之比是( )
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 2:1 |
20.下列关于电解质溶液的叙述正确的是( )
| A. | 若温度不变,在氨水中加入少量NH4Cl固体.氨水的电离度和电离平衡常数均变小 | |
| B. | 滴加甲基橙显红色的溶液:NH4+、NO3-、I-、Cl-可以大量共存 | |
| C. | 若将等pH、等体积的NaOH溶液和氨水分别加水稀释m倍、n倍.稀释后两种溶液的pH仍相等,m<n | |
| D. | 某温度下,水的离子积常数Kw=10-13,在此温度下,将pH=12的NaOH溶液VaL与pH=2的硫酸VbL混合,所得溶液呈中性,则Va:Vb=10:1 |