题目内容
(1)下列实验操作中正确的有 (填编号).
A.测定溶液的pH值时,要先将pH试纸用水湿润
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.称量氢氧化钠固体时,要将药品放在托盘天平坐盘白纸上
D.过滤操作时,为了加快过滤速度,可用玻璃棒在漏斗中轻轻搅拌
E.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
(2)实验室欲配制100mL0.5mol/L的Na2SO4溶液,试回答下列问题:
①实验中用不到的仪器是 (填编号).
A.烧杯 B.圆底烧瓶 C.100mL容量瓶 D.胶头滴管 E.玻璃棒
②配制时应称取Na2SO4?10H2O g.
③下列操作会使所配溶液的浓度偏大的是 (填编号).
A.在烧杯中溶解搅拌时,不慎溅出少量溶液
B.未将洗涤烧杯内壁的溶液转移到容量瓶
C.将烧杯中溶液转移到容量瓶之前,容量瓶有少量蒸馏水
D.容量瓶中定容时,俯视液面读数
E.将配好的溶液从容量瓶转移到试剂瓶时,有少量溅出.
A.测定溶液的pH值时,要先将pH试纸用水湿润
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.称量氢氧化钠固体时,要将药品放在托盘天平坐盘白纸上
D.过滤操作时,为了加快过滤速度,可用玻璃棒在漏斗中轻轻搅拌
E.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
(2)实验室欲配制100mL0.5mol/L的Na2SO4溶液,试回答下列问题:
①实验中用不到的仪器是
A.烧杯 B.圆底烧瓶 C.100mL容量瓶 D.胶头滴管 E.玻璃棒
②配制时应称取Na2SO4?10H2O
③下列操作会使所配溶液的浓度偏大的是
A.在烧杯中溶解搅拌时,不慎溅出少量溶液
B.未将洗涤烧杯内壁的溶液转移到容量瓶
C.将烧杯中溶液转移到容量瓶之前,容量瓶有少量蒸馏水
D.容量瓶中定容时,俯视液面读数
E.将配好的溶液从容量瓶转移到试剂瓶时,有少量溅出.
考点:配制一定物质的量浓度的溶液
专题:
分析:(1)A.pH试纸不能事先湿润;
B.温度计测量蒸气的温度;
C.氢氧化钠固体具有腐蚀性,易潮解,不能放在滤纸上称量;
D.过滤实验中玻璃棒的作用是引流,搅动漏斗里的液体,容易把滤纸弄破;
E.分液操作时下层液体从下口放出,上层液体从上口倒出;
(2)①根据配制溶液的步骤操作选择所用仪器;
②根据n=cV计算硫酸钠的物质的量,再根据m=nM计算硫酸钠的质量;
③分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
判断对所配溶液浓度影响.
B.温度计测量蒸气的温度;
C.氢氧化钠固体具有腐蚀性,易潮解,不能放在滤纸上称量;
D.过滤实验中玻璃棒的作用是引流,搅动漏斗里的液体,容易把滤纸弄破;
E.分液操作时下层液体从下口放出,上层液体从上口倒出;
(2)①根据配制溶液的步骤操作选择所用仪器;
②根据n=cV计算硫酸钠的物质的量,再根据m=nM计算硫酸钠的质量;
③分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
| n |
| V |
解答:
解:(1)A.pH试纸不能事先湿润,否则会带来实验误差,故A错误;
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处,故B正确;
C.氢氧化钠固体具有腐蚀性,易潮解,不能放在滤纸上称量,应在玻璃器皿中称量,如烧杯,故C错误;
D.过滤实验中玻璃棒的作用是引流,防止液体溅出,用玻璃棒搅动漏斗里的液体,容易把滤纸弄破,使实验失败,起不到过滤的作用,故D错误;
E.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,避免两种液体相互污染,故E正确.
故选BE.
(2)①根据配制溶液的步骤操作选择所用仪器,圆底烧瓶是作为有液体参加的反应容器,故答案为:B;
②n=cV=0.5mol/L×0.1L=0.05mol,m=nM=0.05mol×322g/mol=16.1g,故答案为:16.1;
③A.在烧杯中溶解溶质,搅拌时不慎溅出少量溶液,则Na2SO4有损失,所以n(Na2SO4)偏小,故结果偏小;
B.未将洗涤烧杯内壁的溶液转移入容量瓶,Na2SO4有损失,所以n(Na2SO4)偏小,故结果偏小;
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水,因为定容时也要加水,所以原来容量瓶中有少量蒸馏水无影响;
D.定容时俯视液面,会导致溶液体积偏小,所以Na2SO4溶液的浓度偏大;
E.将配得的溶液从容量瓶转移到干燥、洁净的试剂瓶中时,有少量溅出,导致Na2SO4有损失,所以n(Na2SO4)偏小,故结果偏小;
故答案为:D.
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处,故B正确;
C.氢氧化钠固体具有腐蚀性,易潮解,不能放在滤纸上称量,应在玻璃器皿中称量,如烧杯,故C错误;
D.过滤实验中玻璃棒的作用是引流,防止液体溅出,用玻璃棒搅动漏斗里的液体,容易把滤纸弄破,使实验失败,起不到过滤的作用,故D错误;
E.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,避免两种液体相互污染,故E正确.
故选BE.
(2)①根据配制溶液的步骤操作选择所用仪器,圆底烧瓶是作为有液体参加的反应容器,故答案为:B;
②n=cV=0.5mol/L×0.1L=0.05mol,m=nM=0.05mol×322g/mol=16.1g,故答案为:16.1;
③A.在烧杯中溶解溶质,搅拌时不慎溅出少量溶液,则Na2SO4有损失,所以n(Na2SO4)偏小,故结果偏小;
B.未将洗涤烧杯内壁的溶液转移入容量瓶,Na2SO4有损失,所以n(Na2SO4)偏小,故结果偏小;
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水,因为定容时也要加水,所以原来容量瓶中有少量蒸馏水无影响;
D.定容时俯视液面,会导致溶液体积偏小,所以Na2SO4溶液的浓度偏大;
E.将配得的溶液从容量瓶转移到干燥、洁净的试剂瓶中时,有少量溅出,导致Na2SO4有损失,所以n(Na2SO4)偏小,故结果偏小;
故答案为:D.
点评:本题考查了一定物质的量浓度溶液的配制,要注意仪器的选择,误差分析,难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
用胆矾(化学式为CuSO4?5H2O,分子量为250)配制0.1mol/L的水溶液,下列方法正确的是( )
| A、取25 g CuSO4?5H2O溶于1 L水中 |
| B、将CuSO4?5H2O干燥去掉结晶水,取16g溶于水制成1 L溶液 |
| C、将25 g CuSO4?5H2O溶于水制成1 L溶液 |
| D、将16 gCuSO4?5H2O溶于水配成1 L溶液 |
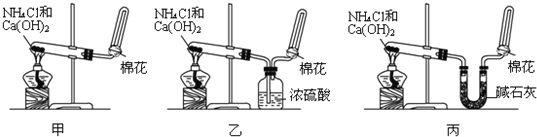
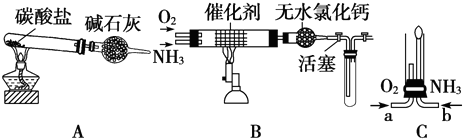
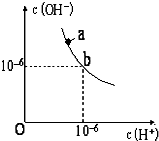 回答下列问题.
回答下列问题.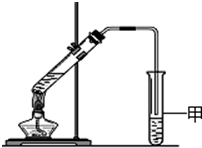 通过粮食发酵可获得某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%.
通过粮食发酵可获得某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%.
