题目内容
将一定量的 SO2 和0.7mol氧气放入5L恒容的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2
2SO3△H<0.反应3min后达到平衡,此时SO2和SO3的总物质的量为1mol;剩余O2体积为5.6L(标准状况下).
请回答下列问题:
(1)最开始充入的SO2 物质的量为 mol.
(2)达到平衡过程O2中的平均反应速率为 .
(3)求该反应达到平衡时SO2的转化率(要求写出计算过程).
| 催化剂 |
| △ |
请回答下列问题:
(1)最开始充入的SO2 物质的量为
(2)达到平衡过程O2中的平均反应速率为
(3)求该反应达到平衡时SO2的转化率(要求写出计算过程).
考点:化学平衡的计算
专题:化学平衡专题
分析:依据化学平衡三段式列式计算,剩余O2体积为5.6L物质的量
=0.25mol
2SO2 +O 2 =2SO3
起始量(mol) n 0.7 0
变化量(mol) 0.9 0.45 0.9
平衡量(mol) n-0.9 0.25 0.9
平衡后SO2和SO3的总物质的量为1mol
(1)n-0.9+0.9=1,n=1mol;
(2)v=
计算分析;
(3)转化率=
×100%.
| 5.6L |
| 22.4L/mol |
2SO2 +O 2 =2SO3
起始量(mol) n 0.7 0
变化量(mol) 0.9 0.45 0.9
平衡量(mol) n-0.9 0.25 0.9
平衡后SO2和SO3的总物质的量为1mol
(1)n-0.9+0.9=1,n=1mol;
(2)v=
| △c |
| △t |
(3)转化率=
| 消耗量 |
| 起始量 |
解答:
解:剩余O2体积为5.6L物质的量
=0.25mol,则
2SO2 +O 2 =2SO3
起始量(mol) n 0.7 0
变化量(mol) 0.9 0.45 0.9
平衡量(mol) n-0.9 0.25 0.9
(1)平衡后SO2和SO3的总物质的量为1mol,n-0.9+0.9=1,n=1mol,故答案为:1;
(2)达到平衡过程O2中的平均反应速率v=
=
=0.03mol/(L?min),故答案为:0.03mol/(L?min);
(3)平衡时SO2的转化率=
×100%=
×100%=90%,故答案为:90%.
| 5.6L |
| 22.4L/mol |
2SO2 +O 2 =2SO3
起始量(mol) n 0.7 0
变化量(mol) 0.9 0.45 0.9
平衡量(mol) n-0.9 0.25 0.9
(1)平衡后SO2和SO3的总物质的量为1mol,n-0.9+0.9=1,n=1mol,故答案为:1;
(2)达到平衡过程O2中的平均反应速率v=
| △c |
| △t |
| ||
| 3min |
(3)平衡时SO2的转化率=
| 消耗量 |
| 起始量 |
| 0.9mol |
| 1mol |
点评:本题考查了化学方程式的计算分析应用,主要是三段式列式计算的过程分析,反应速率、转化率概念的计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
下列原理正确且离子方程式也正确的是( )
| A、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| B、Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
| C、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
| D、0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4+AlO2-+2H2O |
下列有关说法正确的是( )
| A、常温下Ksp(Ag2CrO4)=1.1×10-12,Ksp(AgCl)=1.8×10-10,则Ag2CrO4的溶解度小于AgCl |
| B、纯碱溶于热水中,去油污效果增强,说明纯碱的水解是放热反应 |
| C、为保护海轮的船壳,常在船壳上镶入锌块 |
| D、以熔融Al2O3为电解质进行电解冶炼铝,熔融体中Al3+向阳极移动 |
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
| A、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1 452 kJ?mol-1 |
| B、CH3OH(l)+1.5O2(g)=CO2(g)+2H2O(g)△H=-725.8 kJ?mol-1 |
| C、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-725.8 kJ?mol-1 |
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=+1 452 kJ?mol-1 |
同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是:①NO和O2,②N2和NO2,③NH3和NO,现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是( )
| A、V1>V2>V3 |
| B、V1>V3>V2 |
| C、V2>V3>V1 |
| D、V3>V1>V2 |
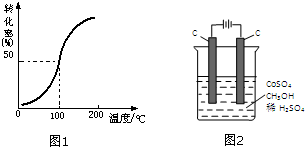 甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.
甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.