题目内容
 甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.
甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.已知:I:CH3OH (g)+
| 1 |
| 2 |
Ⅱ:2H2(g)+O2 (g)═2H2O(g)△△H2=-241.8kJ/mol
(1)甲醇蒸气与水蒸气反应生成CO2(g) 与 H2(g)的热化学方程式为
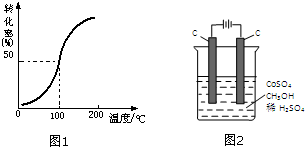
(2)将1.0mol CH3OH (g)和2.0mol O2 ( g )通入容积为10L的反应器,在一定条件下发生反应I,测得在一定压强下CH3OH (g)的平衡转化率与温度的关系如图1.假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平均反应速率为v(H2)=
(3)在某温度和压强下,将一定量 H2与O2充入密闭容器发生反应Ⅱ,平衡后压缩容器体积至原来的
| 1 |
| 2 |
a.平衡常数K增大; b.正反应速率加快,逆反应速率减慢; c.重新平衡c( H2 )/c(H2O )减小.
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+).现用图2装置模拟上述过程,则:
Co2+在阳极的电极反应式为:
(5)甲醇在催化剂条件下可以直接氧化成甲酸.在常温下,用0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH)
考点:化学平衡的计算,热化学方程式,电解原理
专题:
分析:(1)依据热化学方程式和盖斯定律计算所需热化学方程式;
(2)100℃时达到平衡时,甲烷转化率为50%,结合化学平衡三段式列式计算平衡时各组分的物质的量,根据c=
计算v(H2);平衡常数等于生成物平衡浓度幂次方乘积除以反应物幂次方乘积;
(3)其他条件不变,平衡后将容器的容积压缩到原来的
,压强增大,正、逆反应速率都增大,但正反应速率增大更多,平衡向正反应方向移动,生成物的浓度增大,由于温度不变,则平衡常数不变,结合平衡常数可知,平衡时反应物各组分的浓度都增大,据此分析解答;
(4)通电后,将Co2+氧化成Co3+,电解池中阳极失电子发生氧化反应,电极反应为Co2+-e-=Co3+;
以Co3+做氧化剂把水中的甲醇氧化成CO2而净化,自身被还原为Co2+,原子守恒与电荷守恒可知,还原生成H+,配平书写为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
(5)NaOH和甲酸恰好反应时生成强碱弱酸盐,溶液呈碱性,若要呈中性,则甲酸过量.
(2)100℃时达到平衡时,甲烷转化率为50%,结合化学平衡三段式列式计算平衡时各组分的物质的量,根据c=
| ||
| △t |
(3)其他条件不变,平衡后将容器的容积压缩到原来的
| 1 |
| 2 |
(4)通电后,将Co2+氧化成Co3+,电解池中阳极失电子发生氧化反应,电极反应为Co2+-e-=Co3+;
以Co3+做氧化剂把水中的甲醇氧化成CO2而净化,自身被还原为Co2+,原子守恒与电荷守恒可知,还原生成H+,配平书写为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
(5)NaOH和甲酸恰好反应时生成强碱弱酸盐,溶液呈碱性,若要呈中性,则甲酸过量.
解答:
解:(1)I:CH3OH (g)+
O2 (g)═CO2(g)+2H2(g)△H1=-192.9kJ/mol
Ⅱ:2H2(g)+O2 (g)═2H2O(g)△H2=-241.8kJ/mol
依据盖斯定律Ⅰ-Ⅱ×
得到CH3OH (g)+H2O (g)=CO2(g)+3 H2(g)△H=-72.0kJ/mol;
故答案为:CH3OH (g)+H2O (g)=CO2(g)+3 H2(g)△H=-72.0kJ/mol;
(2)将1.0mol CH3OH和2.0mol O2 ( g )通入容积固定为10L的反应室,在一定条件下发生反应I,由图象可知100℃甲醇转化率为50%,故参加反应的甲醇为1mol×50%=0.5mol,则:
CH3 OH(g)+
O2 (g)=CO2 (g)+2H2 (g)
起始量(mol):1.0 2.0 0 0
变化量(mol):0.5 0.25 0.5 1.0
平衡量(mol):0.5 1.75 0.5 1.0
假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平均反应速率=
=0.02 mol?L-1?min-1,该反应的平衡常数表达式为K=
故答案为:0.02;
;
(3)a.平衡常数只受温度影响,温度不变,平衡常数不变,故a错误;
b.压强增大,正、逆反应速率都增大,但正反应速率增大更多,故b错误;
c.压强增大,平衡向正反应方向移动,氢气的物质的量减小、甲醇的物质的量增大,故重新平衡
减小,故c正确;
故答案为:c;
(4)通电后,将Co2+氧化成Co3+,电解池中阳极失电子发生氧化反应,电极反应为Co2+-e-=Co3+;
以Co3+做氧化剂把水中的甲醇氧化成CO2而净化,自身被还原为Co2+,结合原子守恒与电荷守恒可知,还原生成H+,配平书写离子方程式为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
故答案为:Co2+-e-=Co3+;6Co3++CH3OH+H2O=CO2↑+6Co2++6H+.
(5)NaOH和甲酸恰好反应时生成强碱弱酸盐,溶液呈碱性,若要呈中性,则甲酸过,所以滴定到pH=7时,V(NaOH)<20.00ml,故答案为:<;
| 1 |
| 2 |
Ⅱ:2H2(g)+O2 (g)═2H2O(g)△H2=-241.8kJ/mol
依据盖斯定律Ⅰ-Ⅱ×
| 1 |
| 2 |
故答案为:CH3OH (g)+H2O (g)=CO2(g)+3 H2(g)△H=-72.0kJ/mol;
(2)将1.0mol CH3OH和2.0mol O2 ( g )通入容积固定为10L的反应室,在一定条件下发生反应I,由图象可知100℃甲醇转化率为50%,故参加反应的甲醇为1mol×50%=0.5mol,则:
CH3 OH(g)+
| 1 |
| 2 |
起始量(mol):1.0 2.0 0 0
变化量(mol):0.5 0.25 0.5 1.0
平衡量(mol):0.5 1.75 0.5 1.0
假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平均反应速率=
| ||
| 5min |
| c(CO2)c2(H2) | ||
c(CH3OH)c
|
故答案为:0.02;
| c(CO2)c2(H2) | ||
c(CH3OH)c
|
(3)a.平衡常数只受温度影响,温度不变,平衡常数不变,故a错误;
b.压强增大,正、逆反应速率都增大,但正反应速率增大更多,故b错误;
c.压强增大,平衡向正反应方向移动,氢气的物质的量减小、甲醇的物质的量增大,故重新平衡
| c(H2) |
| c(CH3OH) |
故答案为:c;
(4)通电后,将Co2+氧化成Co3+,电解池中阳极失电子发生氧化反应,电极反应为Co2+-e-=Co3+;
以Co3+做氧化剂把水中的甲醇氧化成CO2而净化,自身被还原为Co2+,结合原子守恒与电荷守恒可知,还原生成H+,配平书写离子方程式为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
故答案为:Co2+-e-=Co3+;6Co3++CH3OH+H2O=CO2↑+6Co2++6H+.
(5)NaOH和甲酸恰好反应时生成强碱弱酸盐,溶液呈碱性,若要呈中性,则甲酸过,所以滴定到pH=7时,V(NaOH)<20.00ml,故答案为:<;
点评:本题考查热化学方程式书写、化学平衡图象、影响化学平衡因素、平衡常数与反应速率计算、原电池等,掌握基础是解本题的关键,题目难度中等.

练习册系列答案
相关题目
下列各组实验需水浴加热的是( )
①实验室制乙烯 ②制乙酸乙酯 ③制硝基苯 ④制酚醛树酯 ⑤银镜反应 ⑥制溴苯.
①实验室制乙烯 ②制乙酸乙酯 ③制硝基苯 ④制酚醛树酯 ⑤银镜反应 ⑥制溴苯.
| A、①②③④ | B、②③⑤ |
| C、③④⑤ | D、④⑤⑥ |
下列热化学方程式中,△H能正确表示物质的燃烧热或中和热的是( )
| A、C8H18(l)+12.5O2 (g)=8CO2 (g)+9H2O(l)△H=-5518 kJ?mol-1 |
| B、KOH(aq)+CH3COOH (aq)=CH3COOK(aq)+H2O(l)△H=-57.3 kJ?mol-1 |
| C、2H2(g)+O2(g)=2H2O(l)△H=-572kJ?mol-1 |
| D、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-533kJ?mol-1 |
NaHS、MgSO4、NaHSO4三种物质组成的混合物中,已知氧元素的质量分数为a%,则其中硫元素的质量分数为( )
| A、a% | ||
| B、1-1.75 a% | ||
C、
| ||
D、
|