题目内容
17.NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是Al3+水解生成的Al(OH)3胶体,具有吸附性,即Al3++3H2O═Al(OH)3胶体+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水(用必要的化学用语和相关文字说明).
(2)相同条件下,0.1mol•L-1NH4Al(SO4)2中c(NH4+)大于(填“等于”、“大于”或“小于”)0.1mol•L-1NH4HCO3中c(NH4+).
(3)如图1是0.1mol•L-1电解质溶液的pH随温度变化的图象.
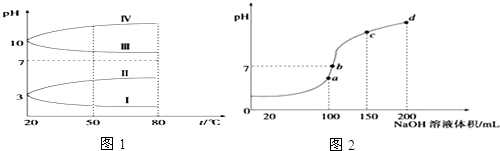
①其中符合0.1mol•L-1NH4Al(SO4)2的pH随温度变化的曲线是I(填写字母),导致pH随温度变化的原因是NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
②20℃时,0.1mol•L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=10-3 mol/L.
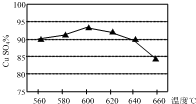
(4)室温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示,试分析图中a、b、c、d四个点,水的电离程度最大的是a;在b点,溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)..
分析 (1)Al3+水解生成的Al(OH)3胶体,具有吸附性;
(2)NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HCO3-和NH4+发生双水解;
(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
②根据电荷守恒定律解题.
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离.b点溶液呈中性.
解答 解:(1)Al3+水解生成的Al(OH)3胶体,具有吸附性,离子方程式:Al3++3H2O═Al(OH)3胶体+3H+,
故答案为:Al3+水解生成的Al(OH)3胶体,具有吸附性,即Al3++3H2O═Al(OH)3胶体+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水;
(2)NH4Al(SO4)2与NH4HCO3中的NH4+均发生水解,但是NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HCO3-和NH4+发生双水解,所以NH4HCO3中NH4+水解程度比NH4Al(SO4)2中的大,则c(NH4+)更小,故答案为:大于;
(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为Ⅰ,
故答案为:Ⅰ;NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
②根据电荷守恒,可以求出2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol•L-1[c(OH-)太小,可忽略],故答案为:10-3 mol/L;
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离.b点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三种成分,a点时c(Na+)=c(SO42-),b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),
故答案为:a;c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
点评 本题考查盐类的水解和离子浓度大小的比较,题目难度中等,(2)②为易错点,注意根据守恒思想解题.

| A. | 不确定 | B. | 变小 | C. | 不变 | D. | 变大 |
| A. | x=2.25 y=4.74% | B. | x=5 y=11.11% | ||
| C. | x=5 y=10% | D. | x=2.875 y=5.75% |
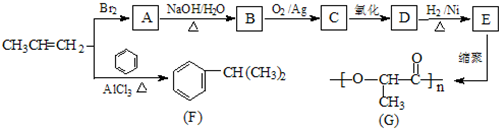
 将某黄铜矿(主要成分为CuFeS2)和O2在一定温度范围内发生反应,反应所得固体混合物X中含有CuSO4、FeSO4、Fe2(SO4)3及少量SiO2等,除杂后可制得纯净的胆矾晶体(CuSO4•5H2O).
将某黄铜矿(主要成分为CuFeS2)和O2在一定温度范围内发生反应,反应所得固体混合物X中含有CuSO4、FeSO4、Fe2(SO4)3及少量SiO2等,除杂后可制得纯净的胆矾晶体(CuSO4•5H2O).(1)实验测得温度对反应所得固体混合物中水溶性铜(CuSO4)的含量的影响如图所示.生产过程中应将温度控制在600℃左右,温度升高至一定程度后,水溶性铜含量下降的可能原因是CuSO4发生了分解反应.
(2)如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).实验中可选用的试剂和用品:稀硫酸、3% H2O2溶液、CuO、玻璃棒、精密pH试纸.
| 粒子 | Cu2+ | Fe2+ | Fe3+ |
| 开始沉淀时的pH | 4.7 | 5.8 | 1.9 |
| 完全沉淀时的pH | 6.7 | 9.0 | 3.2 |
②补充完整由反应所得固体混合物X制得纯净胆矾晶体的实验步骤:
第一步:将混合物加入过量稀硫酸,搅拌、充分反应,过滤.
第二步:向滤液中加入稍过量3% H2O2溶液,充分反应.
第三步:向溶液中加入CuO,用精密pH试纸控制pH在3.2~4.7之间,过滤.
第四步:加热浓缩、冷却结晶.
第五步:过滤、洗涤,低温干燥.
(3)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程反应的离子方程式为4CuFeS2+4H++17O2=4Cu2++4Fe3++8SO42-+2H2O.
| 温度 | 973K | 1173K |
| K1 | 1.47 | 2.15 |
| K2 | 2.33 | 1.67 |
(2)现有反应③:CO2(g)+H2(g)?CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=$\frac{[CO][{H}_{2}O]}{[{H}_{2}][C{O}_{2}]}$
(3)根据反应①与②可推导出K1、K2与K3之间的关系式$\frac{{K}_{1}}{{K}_{2}}$.根据此关系式及表中数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应.
| A. | 10g CO和10g N2 | B. | 10g C2H4和10g C3H6 | ||
| C. | 5.6L O2(标准状况)和0.5mol H2O | D. | 224mL He(标准状况)和1.6g CH4 |
 .
.