题目内容
 右图是铜与稀硝酸反应的实验装置图,请回答下列问题:
右图是铜与稀硝酸反应的实验装置图,请回答下列问题:(1)铜与稀硝酸反应的化学方程式
(2)检验该装置气密性的方法是
(3)烧瓶中可观察到的现象是:铜片溶解、
考点:硝酸的化学性质
专题:氮族元素
分析:(1)Cu与稀硝酸反应生成硝酸铜、NO和水,据此书写方程式;
(2)依据装置中气体压强变化来判断气密性;
(3)烧瓶中发生Cu与稀硝酸反应生成硝酸铜、NO和水,结合一氧化氮的性质来回答现象.
(2)依据装置中气体压强变化来判断气密性;
(3)烧瓶中发生Cu与稀硝酸反应生成硝酸铜、NO和水,结合一氧化氮的性质来回答现象.
解答:
解:(1)Cu与稀硝酸反应生成硝酸铜、NO和水,反应的化学方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
(2)检验装置气密性的方法:用酒精灯稍加热烧瓶,试管中冒气泡,撤掉酒精灯后,导管中上升一段液柱,表明装置不漏气,故答案为:用酒精灯稍加热烧瓶,试管中冒气泡,撤掉酒精灯后,导管中上升一段液柱,表明装置不漏气;
(3)Cu与稀硝酸反应生成硝酸铜、NO和水,所以金属铜会溶解,溶液中因为生成硝酸铜而变蓝色,一氧化氮遇到空气迅速变为红棕色的二氧化氮,故答案为:溶液变为蓝色;有红棕色气体产生.
(2)检验装置气密性的方法:用酒精灯稍加热烧瓶,试管中冒气泡,撤掉酒精灯后,导管中上升一段液柱,表明装置不漏气,故答案为:用酒精灯稍加热烧瓶,试管中冒气泡,撤掉酒精灯后,导管中上升一段液柱,表明装置不漏气;
(3)Cu与稀硝酸反应生成硝酸铜、NO和水,所以金属铜会溶解,溶液中因为生成硝酸铜而变蓝色,一氧化氮遇到空气迅速变为红棕色的二氧化氮,故答案为:溶液变为蓝色;有红棕色气体产生.
点评:本题考查了硝酸性质,掌握实验基本操作、物质的化学性质是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S.下列说法不正确的是( )
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S.下列说法不正确的是( )| A、该装置将化学能转化为电能 |
| B、电子移动方向是由a极流向b极 |
| C、可以用水代替SO(CH3)2做溶剂 |
| D、b极反应式是FeS2+4Li++4e-=Fe+2Li2S |
下列实验不能达到目的是( )
| A、向Na2SiO3溶液中滴加酚酞,溶液变红,证明Na2SiO3发生了水解反应 |
| B、向HClO溶液中通入SO2,生成H2SO4,证明H2SO4的酸性比HClO强 |
| C、将铝箔在酒精灯火焰上加热,铝箔熔化但不滴落,证明氧化铝的熔点高于铝 |
| D、将饱和氯水滴到蓝色石蕊试纸上,试纸先变红后褪色,证明氯水具有漂白性 |
对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A、达到化学平衡时,4v正(O2)=5v逆(NO) |
| B、若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| C、达到化学平衡时,若增加容器体积,则正反应速率增大,逆反应速率减小,平衡正向移动 |
| D、化学反应速率关系是:2v正(NH3)=3v正(H2O) |

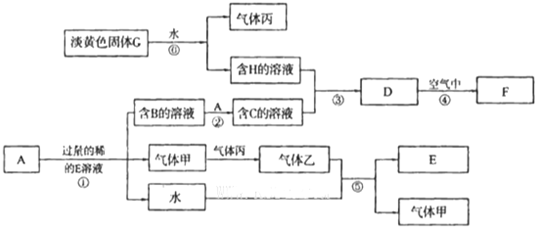
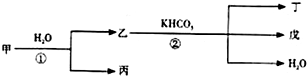 甲、乙、丙、丁、戊几种中学常见的物质在常温有如图转化关系,在转化过程中,乙与KHCO3按等物质的量混合,并且恰好完全反应.
甲、乙、丙、丁、戊几种中学常见的物质在常温有如图转化关系,在转化过程中,乙与KHCO3按等物质的量混合,并且恰好完全反应.