题目内容
已知金属单质A是生产生活中用量最大的金属.D是难溶于水的白色固体.F为红褐色固体.无色气体甲遇气体丙立即生成红棕色的气体乙(图中部分产物和反应的条件略).
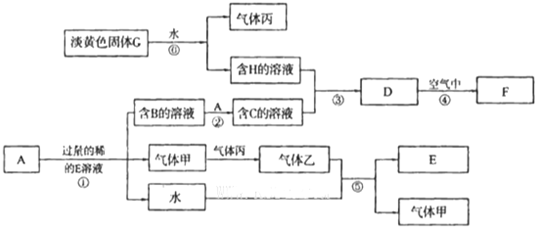
请根据以上信息回答下列问题:
(1)写出下列物质的化学式C G .
(2)写出反应①的化学方程式 .反应②的离子方程式 .
(3)反应④整个过程观察到的现象为 .
(4)反应⑤中,若将充满气体乙的试管倒扣在水槽中,充分反应后,试管内液体占试管总体积 .
(5)某种贫血症患者应补充C物质的阳离子.含该离子的药片外表包有一层特殊的糖衣,这层糖衣的作用就是保护该离子不被空气中的氧气氧化.为检验长期放置的药片已经失效,将药片去除糖衣后研碎,取少量研碎的药片放入烧杯中,加适量的蒸馏水,然后滴加数滴 溶液,溶液显 色,表明该药片已失效.

请根据以上信息回答下列问题:
(1)写出下列物质的化学式C
(2)写出反应①的化学方程式
(3)反应④整个过程观察到的现象为
(4)反应⑤中,若将充满气体乙的试管倒扣在水槽中,充分反应后,试管内液体占试管总体积
(5)某种贫血症患者应补充C物质的阳离子.含该离子的药片外表包有一层特殊的糖衣,这层糖衣的作用就是保护该离子不被空气中的氧气氧化.为检验长期放置的药片已经失效,将药片去除糖衣后研碎,取少量研碎的药片放入烧杯中,加适量的蒸馏水,然后滴加数滴
考点:无机物的推断
专题:推断题
分析:A是生产生活中用量最大的金属,D为Fe,F为红褐色固体,则F为Fe2O3,由转化关系可知,反应①为Fe与过量稀硝酸的反应,B为Fe(NO3)3,C为Fe(NO3)2,气体甲为NO,甲遇气体丙立即生成红棕色的气体乙,气体乙为NO2,则丙为氧气,所以淡黄色固体G为Na2O2,H为NaOH,D为Fe(OH)2,F为Fe(OH)3,然后结合元素化合物性质及化学用语来解答.
解答:
解:A是生产生活中用量最大的金属,D为Fe,F为红褐色固体,则F为Fe2O3,由转化关系可知,反应①为Fe与过量稀硝酸的反应,B为Fe(NO3)3,C为Fe(NO3)2,气体甲为NO,甲遇气体丙立即生成红棕色的气体乙,气体乙为NO2,则丙为氧气,所以淡黄色固体G为Na2O2,H为NaOH,D为Fe(OH)2,F为Fe(OH)3,
(1)由上述分析可知,C为Fe(NO3)2,G为Na2O2,故答案为:Fe(NO3)2;Na2O2;
(2)反应①的化学方程式为Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,反应②的离子方程式为2Fe3++Fe=3Fe2+,
故答案为:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O;2Fe3++Fe=3Fe2+;
(3)反应④发生氢氧化亚铁被氧化为氢氧化铁的反应,则整个过程观察到的现象为白色沉淀迅速变为灰绿色,最后变为红褐色,
故答案为:白色沉淀迅速变为灰绿色,最后变为红褐色;
(4)反应⑤发生3NO2+H2O=2HNO3+NO,只有NO不溶于水,则充满气体乙的试管倒扣在水槽中,充分反应后,试管内液体占试管总体积的
,故答案为:
;
(5)亚铁离子被氧化生成铁离子,遇KSCN溶液变为血红色,则取少量研碎的药片放入烧杯中,加适量的蒸馏水,然后滴加数滴KSCN(或NH4SCN)溶液,溶液显红色,表明该药片已失效,故答案为:KSCN(或NH4SCN);红.
(1)由上述分析可知,C为Fe(NO3)2,G为Na2O2,故答案为:Fe(NO3)2;Na2O2;
(2)反应①的化学方程式为Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,反应②的离子方程式为2Fe3++Fe=3Fe2+,
故答案为:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O;2Fe3++Fe=3Fe2+;
(3)反应④发生氢氧化亚铁被氧化为氢氧化铁的反应,则整个过程观察到的现象为白色沉淀迅速变为灰绿色,最后变为红褐色,
故答案为:白色沉淀迅速变为灰绿色,最后变为红褐色;
(4)反应⑤发生3NO2+H2O=2HNO3+NO,只有NO不溶于水,则充满气体乙的试管倒扣在水槽中,充分反应后,试管内液体占试管总体积的
| 2 |
| 3 |
| 2 |
| 3 |
(5)亚铁离子被氧化生成铁离子,遇KSCN溶液变为血红色,则取少量研碎的药片放入烧杯中,加适量的蒸馏水,然后滴加数滴KSCN(或NH4SCN)溶液,溶液显红色,表明该药片已失效,故答案为:KSCN(或NH4SCN);红.
点评:本题为框图型无机物推断题,完成此类题目,注意把握题干提供的信息并结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式,涉及铁及其化合物及钠及其化合物性质及转化的考查,综合性较强,题目难度中等.

练习册系列答案
相关题目
甲醛(CH2O)、乙酸(C2H4O2)、和丙酸(C3H6O2)组成的混合物中,氧元素的质量分数为44%,则碳元素的质量分数为( )
| A、44% | B、48% |
| C、56% | D、无法计算 |
通过NOx传感器可监测NOx的含量,其工作原理示意图如图,下列说法正确的是( )
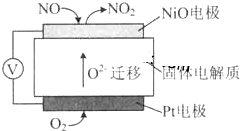

| A、NiO电极是该电池的正极 |
| B、Pt电极附近的pH增大 |
| C、NiO电极的电极反应式:NO-2e-+O2-═NO2 |
| D、固体电解质中O2-向正极移动 |
以下离子方程式的书写正确的是( )
| A、氧化铁和稀盐酸:FeO+2H+=Fe2++H2O |
| B、向NaOH溶液中通Cl2:2OH-+Cl2=Cl-+ClO-+H2O |
| C、向AlCl3溶液中加过量强碱:Al3++3OH-=Al(OH)3↓ |
| D、给漂白粉溶液中加入盐酸:Ca(ClO2)+2H+=2HClO+Ca2+ |
下列各组微粒,在溶液中能大量共存的是( )
| A、K+、H+、NO3-、Cl- |
| B、Cu2+、Cl-、OH-、SO42- |
| C、H+、Na+、HCO3-、Cl- |
| D、Ca2+、Cl-、K+、CO32- |
 右图是铜与稀硝酸反应的实验装置图,请回答下列问题:
右图是铜与稀硝酸反应的实验装置图,请回答下列问题: