题目内容
在下列反应中,HCl做还原剂的是( )
| A、Zn+2HCl=H2↑+ZnCl2 | ||||
| B、CaCO3+2HCl=CO2↑+CaCl2+H2O | ||||
C、MnO2+4HCl(浓)
| ||||
| D、HCl+KOH=KCl+H2O |
考点:氧化还原反应
专题:氧化还原反应专题
分析:HCl作还原剂,说明HCl中元素失电子化合价升高,据此分析解答.
解答:
解:A.该反应中H元素化合价由+1价变为0价,得电子化合价降低,作氧化剂,故A错误;
B.该反应中没有元素化合价变化,不属于氧化还原反应,故B错误;
C.该反应中Cl元素化合价由-1价变为0价,则HCl失电子作还原剂,故C正确;
D.该反应中没有元素化合价变化,不属于氧化还原反应,属于复分解反应,故D错误;
故选C.
B.该反应中没有元素化合价变化,不属于氧化还原反应,故B错误;
C.该反应中Cl元素化合价由-1价变为0价,则HCl失电子作还原剂,故C正确;
D.该反应中没有元素化合价变化,不属于氧化还原反应,属于复分解反应,故D错误;
故选C.
点评:本题考查了氧化还原反应,根据元素化合价是否变化来分析解答,熟悉常见元素化合价,题目难度不大.

练习册系列答案
相关题目
欲增大铁与酸反应放出氢气的速率,下列措施中不正确的是( )
| A、用铁粉代替铁片 |
| B、提高反应温度 |
| C、用浓硫酸代替稀硫酸 |
| D、去除铁表面的铁锈 |
从理论上分析,碳原子数小于10的烷烃分子中,其一卤代物不存在同分异构体的烷烃分子共有的种数是( )
| A、3 | B、4 | C、5 | D、6 |
下列离子方程式正确的是( )
| A、Fe3O4与稀硝酸反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| B、SO2通入Ba(NO3)2溶液中:Ba2++SO2+H2O=BaSO3↓+2H+ |
| C、硫酸铵溶液与Ba(OH)2溶液反应:Ba2++SO42-=BaSO4↓ |
| D、FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 |
在空气中既不易被氧化,也不易分解,且可以用无色玻璃瓶存放的药品是( )
| A、硝酸银 | B、钠 |
| C、浓硝酸 | D、浓硫酸 |
有如图装置,下列有关该装置反应开始时的叙述正确的是( )
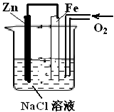

| A、锌极附近滴入酚酞,溶液呈红色 |
| B、铁极发生的电极反应为:2H2O+O2+4e═4OH- |
| C、铁极发生吸氧腐蚀生成锈蚀 |
| D、溶液中的OH-离子向铁极移动 |
下列各装置中,烧杯中盛有海水,能够形成原电池并且铁为正极的是( )
A、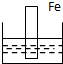 |
B、 |
C、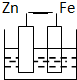 |
D、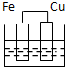 |
下列溶液中,阴离子浓度最大的是( )
| A、0.5mol/L HCl溶液50mL |
| B、0.6mol/L Al2(SO4)3溶液40mL |
| C、0.7mol/L NaCl溶液70mL |
| D、0.8mol/L Na2CO3溶液60mL |
将过量Cl2通入NaBr和NaI的混合液中,然后把混合溶液蒸干,再将剩余残渣灼烧,最后留下的物质( )
| A、NaBr,NaI |
| B、NaCl,NaBr |
| C、NaCl |
| D、NaCl,I2 |