题目内容
20.已知:①能量越低的物质就越稳定,②白磷转化成红磷是放热反应.据此,下列判断或说法中正确的是( )| A. | 在相同的条件下,红磷比白磷稳定 | |
| B. | 在相同的条件下,白磷比红磷稳定 | |
| C. | 红磷和白磷的化学性质相同 | |
| D. | 红磷容易发生自燃而白磷则不会自燃 |
分析 根据能量越低的物质就越稳定,白磷转化成红磷是放热反应,则红磷的能量低,红磷稳定,据此进行解答.
解答 解:A.白磷转化成红磷是放热反应,故红磷的能量低,红磷稳定,故A正确;
B.红磷的能量低,红磷稳定,故B错误;
C.红磷和白磷的结构不同,则二者化学性质不同,故C错误;
D.红磷不容易发生自燃而白磷容易自燃,故D错误;
故选A.
点评 本题考查反应热与焓变的应用,题目难度不大,明确物质稳定性与具有能量的关系为解答关键,注意掌握化学反应与能量变化的关系.

练习册系列答案
相关题目
5.自2016 年1月确定113号、115号、117号和118号元素的命名权起,元素周期表第七周期即被填满. 根据所学知识,第七周期中第一电离能(I1)比115号元素大的主族元素有( )种.
| A. | 1 | B. | 2 | C. | 3 | D. | 不能确定 |
12.下列物质中不能由两种单质直接化合得到的是( )
| A. | FeCl3 | B. | Cu2S | C. | SO3 | D. | NH3 |
9.${\;}_{6}^{12}$C、${\;}_{6}^{13}$C和${\;}_{6}^{14}$C,它们之间的关系是( )
| A. | 同系物 | B. | 同位素 | C. | 同分异构体 | D. | 同素异形体 |
10.将8.4g铁粉和3.2g硫粉混合均匀,加热到反应完全为止,冷却后加足量盐酸,收集到的气体在标准状况时的体积为( )
| A. | 1.12L | B. | 2.24L | C. | 3.36L | D. | 4.48L |

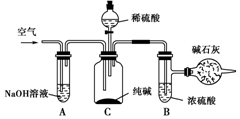 工业纯碱中常含有NaCl、Na2SO4等杂质,可用如图所示的装置测定工业纯碱中有效成分的含量.
工业纯碱中常含有NaCl、Na2SO4等杂质,可用如图所示的装置测定工业纯碱中有效成分的含量.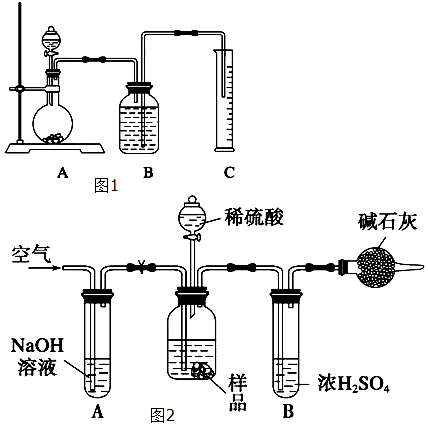
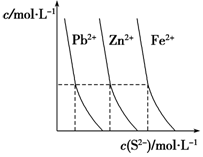 高中化学涉及的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡等,它们在工农业生产中都有广泛的应用.请回答下列问题:
高中化学涉及的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡等,它们在工农业生产中都有广泛的应用.请回答下列问题: