题目内容
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)? ?4NO2(g)+O2(g) ΔH>0
?4NO2(g)+O2(g) ΔH>0
T1温度下的部分实验数据为:
t/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
C
【解析】
试题分析:由速率公式求算出N2O5分解速率为 =2.96×10-3 mol·(L·s)-1,A正确;K1=[(5.0mol/l)4×(1.25mol/l)]/(2.5mol/l)2=125,1000s时转化率为50%,B正确;其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,说明平衡往逆反应方向移动,则T1>T2,C错误。温度升高平衡常数增加,若K1>K3,则T1>T3,D正确。答案选C.
=2.96×10-3 mol·(L·s)-1,A正确;K1=[(5.0mol/l)4×(1.25mol/l)]/(2.5mol/l)2=125,1000s时转化率为50%,B正确;其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,说明平衡往逆反应方向移动,则T1>T2,C错误。温度升高平衡常数增加,若K1>K3,则T1>T3,D正确。答案选C.
考点:化学反应速率、化学平衡常数

(9分)化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,5 g甲醇(CH3OH,液态)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,试写出甲醇燃烧的热化学方程式: 。
(2)已知化学键的键能为:
化学键 | H—H | N—H |
|
键能/( kJ·mol-1) | 436 | 391 | 945 |
又知反应N2(g)+3H2(g)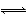 2NH3(g) ΔH=a kJ·mol-1。试根据表中所列键能数据估算a的值为 。
2NH3(g) ΔH=a kJ·mol-1。试根据表中所列键能数据估算a的值为 。
(3)已知:C(石墨,s)+O2(g) CO2(g) ΔH=-393 kJ·mol-1
CO2(g) ΔH=-393 kJ·mol-1
2H2(g)+O2(g) 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1
2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l) ΔH=-2599 kJ·mol-1
4CO2(g)+2H2O(l) ΔH=-2599 kJ·mol-1
根据盖斯定律,计算298 K时C(石墨,s)和H2(g)反应生成1 mol C2H2(g)的焓变为 。
 2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(假定测量过程中没有能量损失):
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(假定测量过程中没有能量损失):

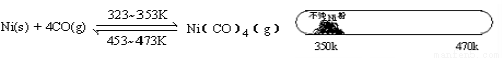

 ,该有机物中含氧官能团有: 、 、 、 (写官能团名称)。
,该有机物中含氧官能团有: 、 、 、 (写官能团名称)。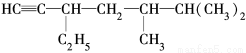 的系统名称是 ,将其在催化剂存在下完全氢化,所得烷烃的系统名称是 。
的系统名称是 ,将其在催化剂存在下完全氢化,所得烷烃的系统名称是 。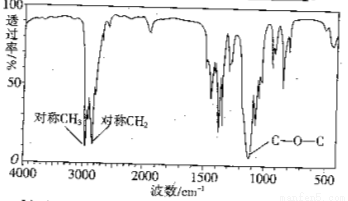
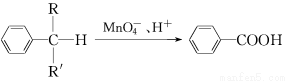
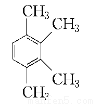 、 、 、 。
、 、 、 。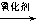 RCOOH+R,COOH。写出
RCOOH+R,COOH。写出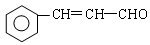 在强氧化剂条件下生成
在强氧化剂条件下生成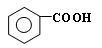 和另一种有机物 (写出其结构简式)。
和另一种有机物 (写出其结构简式)。