题目内容
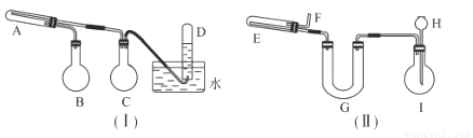
(16分)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉,这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用如图所示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6 mol·L-1的盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去。)
填写下列空白:
(1)实验进行时试管A中应加入的试剂是_________________;烧瓶B的作用是____________;烧瓶C的作用是_______________
(2)实验时,长颈漏斗H中应加入_____________________U型管G的作用是____________
(3)装置I中,在实验时需要加热的仪器是(填该仪器对应的字母)_________ ____ ;
当反应转移了4mol电子时,试管D中收集到的气体在标准状况下的体积为_____________。
(4)写出试管A中发生反应的化学方程式:________________________
(16分)(每空2分)(1)铁粉 ;作为水蒸气发生器(或用来产生水蒸气); 防倒吸(或用作安全瓶)
(2)6 mol·L-1 HCl ;除去H2中混有的HCl和水蒸气;(3)A、B ; 44.8L
(4) 3Fe+4H2O(g)  Fe3O4+4H2。
Fe3O4+4H2。
【解析】
试题分析:(1)在烧瓶A中进行Fe与水蒸气的反应,所以固体Fe放在试管A中。水蒸气通过B加入产生。实验进行时试管A中应加入的试剂是铁粉;烧瓶B的作用是作为水蒸气发生器(或用来产生水蒸气);烧瓶C的作用是 防倒吸(或用作安全瓶) ;(2)在进行氢气与铁的氧化物反应产生颗粒很细的铁粉的实验时,长颈漏斗H中应加入6mol/L的HCl;由于HCl有挥发性,所以在制取的氢气中含有杂质HCl,U型管G的作用是除去H2中混有的HCl和水蒸气;(3)装置I中,使水气化为水蒸气及使水蒸气与炽热的Fe反应的装置都需要加热,因此在实验时需要加热的仪器是A、B ;在装置A中发生反应:3Fe+4H2O(g)  Fe3O4+4H2。根据方程式可知:每产生4mol的氢气,电子转移8mol,所以当反应转移了4mol电子时,试管D中收集到的气体的物质的量是2mol,由于在标准状况下气体摩尔体积是22.4L/mol,所以气体的体积为44.8L;(4)在试管A中发生反应的化学方程式是: 3Fe+4H2O(g)
Fe3O4+4H2。根据方程式可知:每产生4mol的氢气,电子转移8mol,所以当反应转移了4mol电子时,试管D中收集到的气体的物质的量是2mol,由于在标准状况下气体摩尔体积是22.4L/mol,所以气体的体积为44.8L;(4)在试管A中发生反应的化学方程式是: 3Fe+4H2O(g)  Fe3O4+4H2。
Fe3O4+4H2。
考点:考查在Fe与水蒸气反应中装置的作用、物质的使用、方程式的书写及有关物质的量的计算的知识。

N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)? ?4NO2(g)+O2(g) ΔH>0
?4NO2(g)+O2(g) ΔH>0
T1温度下的部分实验数据为:
t/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
温度为T时,向2.0L恒容密闭容器中充入1.0 molPCl5,反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50 s的平均速率为v(PCl3)=0.0032 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,达到平衡时,PCl3的转化率大于80%