题目内容
(9分)化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,5 g甲醇(CH3OH,液态)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,试写出甲醇燃烧的热化学方程式: 。
(2)已知化学键的键能为:
化学键 | H—H | N—H |
|
键能/( kJ·mol-1) | 436 | 391 | 945 |
又知反应N2(g)+3H2(g)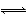 2NH3(g) ΔH=a kJ·mol-1。试根据表中所列键能数据估算a的值为 。
2NH3(g) ΔH=a kJ·mol-1。试根据表中所列键能数据估算a的值为 。
(3)已知:C(石墨,s)+O2(g) CO2(g) ΔH=-393 kJ·mol-1
CO2(g) ΔH=-393 kJ·mol-1
2H2(g)+O2(g) 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1
2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l) ΔH=-2599 kJ·mol-1
4CO2(g)+2H2O(l) ΔH=-2599 kJ·mol-1
根据盖斯定律,计算298 K时C(石墨,s)和H2(g)反应生成1 mol C2H2(g)的焓变为 。
(1) CH3OH (g)+ 3/2O2(g) CO2(g)+2H2O(l) ΔH=-726.4 kJ·mol-1;(2)-93 (3)227.7 kJ·mol-1
CO2(g)+2H2O(l) ΔH=-726.4 kJ·mol-1;(2)-93 (3)227.7 kJ·mol-1
【解析】
试题分析:(1)5gCH3OH在氧气中燃烧生成CO2和液态水,放出113.5kJ热量,32g即1molCH3OH在氧气中燃烧生成CO2和液态水,放出726.4kJ热量,则热化学方程式为:CH3OH (g)+ 3/2O2(g) CO2(g)+2H2O(l) ΔH=-726.4 kJ·mol-1;故答案为:CH3OH (g)+ 3/2O2(g)
CO2(g)+2H2O(l) ΔH=-726.4 kJ·mol-1;故答案为:CH3OH (g)+ 3/2O2(g) CO2(g)+2H2O(l) ΔH=-726.4 kJ·mol-1;(2)N2(g)+3H2(g)??2NH3(g)△H=945kJ?mol-1+436kJ?mol-1×3-391kJ?mol-1×6=-93kJ?mol-1=a kJ?mol-1,因此a=-93,故答案为:-93;已知:①C (s,石墨)+O2(g)=CO2(g)△H1=-393kJ?mol-1;②2H2(g)+O2(g)=2H2O (l)△H2=-571.6kJ?mol-1;③2C2H2(g)+5O2(g)═4CO2(g)+2H2O (l)△H2=-2599kJ?mol-1;2C (s,石墨)+H2(g)=C2H2(g)的反应可以根据①×2+②×
CO2(g)+2H2O(l) ΔH=-726.4 kJ·mol-1;(2)N2(g)+3H2(g)??2NH3(g)△H=945kJ?mol-1+436kJ?mol-1×3-391kJ?mol-1×6=-93kJ?mol-1=a kJ?mol-1,因此a=-93,故答案为:-93;已知:①C (s,石墨)+O2(g)=CO2(g)△H1=-393kJ?mol-1;②2H2(g)+O2(g)=2H2O (l)△H2=-571.6kJ?mol-1;③2C2H2(g)+5O2(g)═4CO2(g)+2H2O (l)△H2=-2599kJ?mol-1;2C (s,石墨)+H2(g)=C2H2(g)的反应可以根据①×2+②×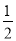 -③
-③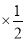 得到,所以反应焓变△H=2×(-393kJ?mol-1)+(-571.6kJ?mol-1)×
得到,所以反应焓变△H=2×(-393kJ?mol-1)+(-571.6kJ?mol-1)× -(-2599kJ?mol-1)×
-(-2599kJ?mol-1)× =+227.7kJ?mol-1,故答案为:+227.7kJ?mol-1;
=+227.7kJ?mol-1,故答案为:+227.7kJ?mol-1;
考点:化学反应中的能量变化

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
则25 ℃时,反应X+3Y? ?2Z的平衡常数为
?2Z的平衡常数为
A.500 B.600 C.1 200 D.1 600
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)? ?4NO2(g)+O2(g) ΔH>0
?4NO2(g)+O2(g) ΔH>0
T1温度下的部分实验数据为:
t/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3

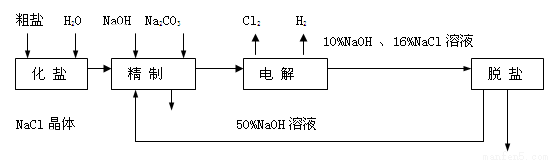
 含量较高,必须添加钡试剂除去SO
含量较高,必须添加钡试剂除去SO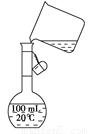
 ?CO (g) + H2(g)在一可变容积的密闭容器中进行,下列条件的改变能加快其反应速率的是
?CO (g) + H2(g)在一可变容积的密闭容器中进行,下列条件的改变能加快其反应速率的是