题目内容
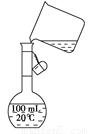
已知298 K时,合成氨反应N2(g)+3H2(g)  2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(假定测量过程中没有能量损失):
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(假定测量过程中没有能量损失):
A.一定大于92.0 kJ B.无法确定
C.一定小于92.0 kJ/mol D.一定小于92.0 kJ
D
【解析】
试题分析:根据热化学方程式,生成2mol氨气放出92.0 kJ的能量,该反应为可逆反应,1 mol N2和3 mol H2放在一密闭容器中,生成氨气的量一定小于2mol,所以放出的能量一定一定小于92.0 kJ,故D项正确。
考点:本题考查反应热。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)? ?4NO2(g)+O2(g) ΔH>0
?4NO2(g)+O2(g) ΔH>0
T1温度下的部分实验数据为:
t/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
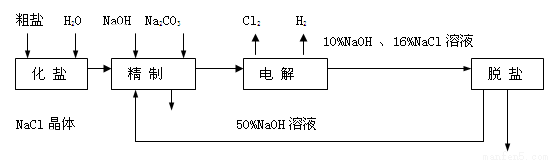
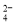 含量较高,必须添加钡试剂除去SO
含量较高,必须添加钡试剂除去SO