题目内容
将铁和铜混合均匀并平均分成四等份,每份13.2g,分别加入同浓度的稀硝酸,充分反应后,在标准状况下生成NO的体积与剩余金属的质量见下表(设硝酸的还原产物只有NO).试通过计算填空:
①写出实验①中发生反应的离子方程式 ;
②实验④中V= .
| 实验编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属质量/g | 9.0 | 4.8 | 0 | 0 |
| NO体积/L | 1.12 | 2.24 | 3.36 | V |
②实验④中V=
考点:离子方程式的有关计算
专题:计算题
分析:①金属铁的活泼性强于铜,根据金属铁和硝酸发生反应的情况来书写;
②先判断酸是否完全反应,再根据金属活动性判断反应的金属及生成的金属离子价态,根据1、2两组数据,结合采用极限法分析,确定剩余固体的成分,据此来计算即可.
②先判断酸是否完全反应,再根据金属活动性判断反应的金属及生成的金属离子价态,根据1、2两组数据,结合采用极限法分析,确定剩余固体的成分,据此来计算即可.
解答:
解:①由①、②两组数据分析,两次剩余物的质量相差4.2g,此时生成1.12LNO气体(转移0.075 mol电子).若只溶解铁,质量为4.2g,若只溶解铜,质量为4.8g.由此可知这9g中是金属Cu,实验①中发生反应的离子方程式为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,
故答案为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O;
②在金属消耗完毕以后,硝酸将亚铁离子氧化为三价铁,在亚铁离子转化为铁离子过程中,结合试验①可知还会产生1.12L的气体,所以试验④中V=4.48L,
故答案为:4.48L.
故答案为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O;
②在金属消耗完毕以后,硝酸将亚铁离子氧化为三价铁,在亚铁离子转化为铁离子过程中,结合试验①可知还会产生1.12L的气体,所以试验④中V=4.48L,
故答案为:4.48L.
点评:本题考查混合物的有关计算,根据表中数据判断各阶段发生的反应是解题关键,侧重对学生综合能力的考查,题目难度中等.

练习册系列答案
相关题目
尼泊金酯是对羟基苯甲酸  与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
 与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )| A、尼泊金乙酯与NaOH溶液反应时,可消耗1mol NaOH |
| B、尼泊金乙酯分子结构中,至少有6个碳原子在一个平面内 |
| C、尼泊金丁酯最多可与4mol H2发生加成反应 |
D、尼泊金丁酯是由对羟基苯甲酸与1-丁醇形成的酯,结构简式如图: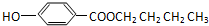 |
下列说法正确的是( )
| A、强电解质溶液导电能力一定比弱电解质溶液导电能力强 |
| B、水的电离过程是吸热过程,升高温度,KW和pH都增大 |
| C、AlCl3和FeCl3既可作净水剂也可作消毒剂 |
| D、将碳酸钠溶液蒸干并灼烧,所得固体的成分仍为碳酸钠 |
求下列溶液的pH(常温条件下)(已知lg2=0.3)
(1)0.005mol?L-1的H2SO4溶液.
(2)已知CH3COOH的电离常数Ka=1.8×10-5,0.1mol?L-1的CH3COOH溶液.
(1)0.005mol?L-1的H2SO4溶液.
(2)已知CH3COOH的电离常数Ka=1.8×10-5,0.1mol?L-1的CH3COOH溶液.
下列各组离子中,能再溶液中大量共存的是( )
| A、Na+、H+、NO3-、Fe2+ |
| B、Ca2+、NO3-、HCO3-、OH- |
| C、K+、H+、Cl-、SO42- |
| D、Fe3+、Cl-、H+、CO32- |
T℃时A气体与B气体反应生成C气体.反应过程中A、B、C浓度(mol/L)随时间变化如图I所示;若保持其他条件不变,温度分别为T1和T2时,C的体积分数与时间的关系如图Ⅱ所示.下列结论正确的是( )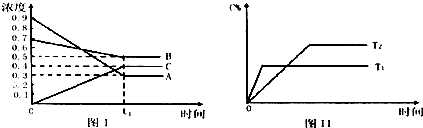

| A、在时间为t1时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B、在时间为t1时,保持温度和压强不变,通入稀有气体,平衡向正反应方向移动 |
| C、其它条件不变,T℃时由0.6 mol/LA、0.6mol/LB、0.2mol/LC开始反应,达到平衡后C的浓度仍为0.4mol/L |
| D、其它条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
下列有关说法正确的是( )
| A、所有氧化还原反应中,氧化剂的氧化性一定强于氧化产物的氧化性 |
| B、根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 |
| C、用酿造C2H5OH作燃料,不会增加大气中CO2含量 |
| D、氟氯烃含量是空气质量报告的主要项目之一 |
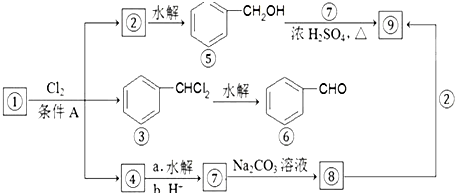
 .如图所示是九种化合物的转变关系.
.如图所示是九种化合物的转变关系.