题目内容
下列说法正确的是( )
| A、摩尔是一个基本物理量 |
| B、CH4的摩尔质量为16g |
| C、在同温同压下,相同体积的任何气体单质所含分子数相同 |
| D、500mL,1mol/L MgCl2溶液中含有Cl-数目为0.5NA |
考点:物质的量的单位--摩尔,摩尔质量,阿伏加德罗常数
专题:
分析:A.摩尔只是物质的量的单位,不是物理量;
B.摩尔质量的单位错误,应该为g/mol;
C.同温同压下,气体摩尔体积相同,则等体积的气体具有相同的物质的量及分子数;
D.氯离子的物质的量浓度为氯化镁的浓度的2倍.
B.摩尔质量的单位错误,应该为g/mol;
C.同温同压下,气体摩尔体积相同,则等体积的气体具有相同的物质的量及分子数;
D.氯离子的物质的量浓度为氯化镁的浓度的2倍.
解答:
解:A.物质的量为基本物理量,而摩尔是物质的量的单位,故A错误;
B.甲烷的摩尔质量为16g/mol,16g为1mol甲烷的质量,故B错误;
C.在同温同压下,气体摩尔体积相同,则相同体积的任何气体单质具有相同的物质的量,所以所含分子数一定相同,故C正确;
D.500mL 1mol/L MgCl2溶液中氯离子浓度为2mol/L,氯离子的物质的量为1mol,含有Cl-数目为NA,故D错误;
故选C.
B.甲烷的摩尔质量为16g/mol,16g为1mol甲烷的质量,故B错误;
C.在同温同压下,气体摩尔体积相同,则相同体积的任何气体单质具有相同的物质的量,所以所含分子数一定相同,故C正确;
D.500mL 1mol/L MgCl2溶液中氯离子浓度为2mol/L,氯离子的物质的量为1mol,含有Cl-数目为NA,故D错误;
故选C.
点评:本题考查了物质的量与摩尔、摩尔质量的关系,题目难度不大,注意掌握物质的量与摩尔质量、物质的量浓度、阿伏伽德罗常数之间的转化关系,明确物质的量与摩尔、相对分子质量与摩尔质量、摩尔质量与质量的区别.

练习册系列答案
相关题目
下列用来表示物质变化的化学用语中,正确的是( )
| A、用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-=Cl2↑ |
| B、在碱性介质中,氢氧燃料电池的负极反应式为O2+2H2O+4e-=4OH- |
| C、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为Cu-2e-=Cu2+ |
| D、钢铁发生电化学腐蚀的正极反应式为Fe-2e-=Fe2+ |
下列说法正确的是( )
| A、钢管与铜管家露天堆放在一起,钢管不易腐蚀 |
| B、生铁浸泡在食盐水中发生析氢腐蚀 |
| C、给铁钉镀铜可采用CuSO4作电镀液 |
| D、电解饱和食盐水时在阳极得到氯气,阴极得到金属钠 |
下列关于反应热的说法正确的是( )
| A、当△H<O时,表示该反应为吸热反应 | ||
B、已知C(s)+
| ||
| C、反应热的大小与反应物所具有的能量和生成物所具有的能量无关 | ||
| D、化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
关于氢键,下列说法正确的是( )
| A、氢键比分子间作用力强,所以它属于化学键 |
| B、冰融化成水的过程中,既破坏了范德华力又破坏了分子间氢键 |
| C、分子形成的氢键一定使物质的熔点和沸点升高 |
| D、测定100℃水蒸气的相对分子质量时发现实验值大于理论值,一定使实验操作不当引起的 |
能正确表示下列化学反应的离子方程式的是( )
| A、铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、铝粉投入到NaOH溶液中:Al+2OH-═AlO2-+H2↑ |
| C、氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
HA为一元弱酸,则在0.1mol?L-1NaA溶液中,离子浓度关系正确的是( )
| A、c(Na+)>c(A-)>c(H+)>c(OH-) |
| B、c(Na+)>c(OH-)>c(A-)>c(H+) |
| C、c(Na+)+c(H+)=c(A-)+c(OH-) |
| D、c(Na+)+c(OH-)=c(A-)+c(H+) |
 (其中R为烃基),相对分子质量为194.工业上以邻二甲苯(
(其中R为烃基),相对分子质量为194.工业上以邻二甲苯( )为原料先生产苯酐(
)为原料先生产苯酐( ),再使其与某醇在一定条件下反应可制得DMP.实验室由以下方法亦可得到DMP:
),再使其与某醇在一定条件下反应可制得DMP.实验室由以下方法亦可得到DMP: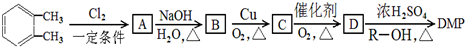
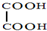 )在一定条件下可以按物质的量1:1发生反应可生成高分子化合物,反应的化学方程式为
)在一定条件下可以按物质的量1:1发生反应可生成高分子化合物,反应的化学方程式为