题目内容
7.下列表示物质形成过程的电子式正确的是( )| A. | 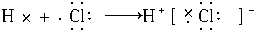 | |
| B. | 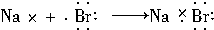 | |
| C. | 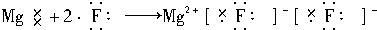 | |
| D. | 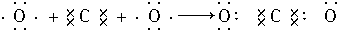 |
分析 化学中常在元素符号周围用小黑点“•”或小叉“×”来表示元素原子的最外层电子,相应的式子叫做电子式,用电子式表示化合物形成过程时,应先判定化合物类型,若为离子化合物,则用箭头表示电子的移动,若为共价化合物,则不需要箭头表示.据此分析.
解答 解:A、HCl属于共价化合物,氢原子最外层电子与Cl最外层电子形成一对共用电子对,其形成过程可写为: ,故A错误;
,故A错误;
B、NaBr属于离子化合物,Na原子最外层电子被Br原子得到,其化合物形成过程为: ,故B错误;
,故B错误;
C、氟离子和镁离子通过离子键形成离子化合物氟化镁,其形成过程为 ,相同离子不能合并,故C错误;
,相同离子不能合并,故C错误;
D、二氧化碳是氧原子和碳原子之间通过共价键形成的共价化合物,形成过程为: ,故D正确.
,故D正确.
故选D.
点评 本题考查了用电子式表示离子化合物、共价化合物的形成过程,题目难度中等,注意掌握电子式的表示方法,能够用电子式表示共价化合物和离子化合物的形成过程.

练习册系列答案
相关题目
4.下列电离方程式书写错误的是( )
| A. | NaHCO3=Na++H++CO32- | B. | NH4NO3=NH4++NO3- | ||
| C. | Na2SO4=2Na++SO42- | D. | Ba(OH)2=Ba2++2OH- |
5.已知:SO32-+I2+H2O═SO42-+2I-+2H+,某无色溶液中可能含有Na+、NH4+、Cu2+、K+、I-、SO32-、SO42-,且所有离子物质的量浓度相等.向溶液中滴加少量氯水,溶液呈无色(不考虑盐类的水解及水的电离).下列关于该溶液的判断正确的是( )
| A. | 肯定不含I- | B. | 不能确定是否含有SO42- | ||
| C. | 至少含有Na+、NH4+、K+中的两种 | D. | 可能含有Cu2+ |
2.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | CaCl2 ? NaOH H2O | D. | NH3 H2O CO2 |
12.下列关于化学键叙述正确的是( )
| A. | 化学键是相邻原子间的相互作用 | |
| B. | 化学键既存在于相邻原子之间,又存在与相邻分子之间 | |
| C. | 化学键通常指的是相邻的两个或多个原子之间的强烈互吸引作用 | |
| D. | 化学键通常是指物质中相邻的原子或离子之间存在的强烈相互作用 |
19.下列说法错误的是( )
| A. | 原子的质量几乎全部集中在原子核上 | |
| B. | 放射性同位素可以用于食物保鲜和肿瘤的治疗 | |
| C. | 在含有多个电子的原子里能量高的电子在离核较近的区域内运动 | |
| D. | ${\;}_{92}^{234}$、${\;}_{92}^{235}$U、${\;}_{92}^{238}$U三种核素互为同位素 |
16.
(1)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥的后面.
(2)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2SO4(或HNO3、H2CO3) | ③NaOH(或KOH) ④Ba(OH)2 | ⑤Na2CO3 ⑥Na2SO4(或K2CO3、Na2SO3) | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(2)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
17.将24g可能含Na、Mg、Al、Fe的合金投入稀HCl中放出氢气的质量为2g,则此合金中一定含( )
| A. | Na | B. | Mg | C. | Al | D. | Fe |