题目内容
16.| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2SO4(或HNO3、H2CO3) | ③NaOH(或KOH) ④Ba(OH)2 | ⑤Na2CO3 ⑥Na2SO4(或K2CO3、Na2SO3) | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(2)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 (1)根据物质的分类和酸碱盐以及氧化物的概念进行分类,含氧酸含有氧元素并能电离出氢离子;碱电离出的阴离子全部为氢氧根离子;盐电离出得阳离子为金属离子,阴离子为酸根离子;氢化物为非金属元素与氢元素组成的化合物.S、N为非金属元素,对应的含氧酸有H2SO4、H2SO3或HNO3 ,K、Na为活泼金属元素,对应的碱有NaOH和KOH,形成的盐为含氧酸盐,有Na2SO4、K2SO3或K2SO4或NaNO3、KNO3、NaNO2、Na2SO3等,氢化物有NH3、H2S;
(2)双氧水在二氧化锰的催化作用下分解可以制得氧气.
解答 解:(1)S、N为非金属元素,对应的含氧酸有H2SO4、H2SO3或HNO3 ,K、Na为活泼金属元素,对应的碱有NaOH和KOH,形成的盐为含氧酸盐,有Na2SO4、K2SO3或K2SO4,
故答案为:②H2SO4(或HNO3、H2CO3);③NaOH(或KOH);⑥Na2SO4(或K2CO3、Na2SO3);
(2)实验室双氧水在二氧化锰的催化作用下分解可以制得氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 本题考查物质的分类,物质组成和概念实质的理解应用,题目难度不大,注意把握相关概念.

练习册系列答案
相关题目
13.下列反应不属于氧化还原反应的是( )
| A. | Cl2+H2O=HCl+HClO | B. | Fe+CuSO4=FeSO4+Cu | ||
| C. | 2NaHCO3 $\frac{\underline{\;△\;}}{\;}$Na2CO3+H2O+CO2 | D. | Cl2+2FeCl2=3FeCl3 |
7.下列表示物质形成过程的电子式正确的是( )
| A. | 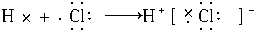 | |
| B. | 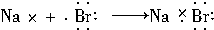 | |
| C. | 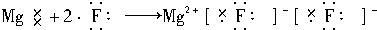 | |
| D. | 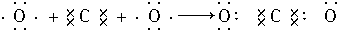 |
11.下列各组物质中,所含原子个数相同的是( )
| A. | 9g水和0.75mol一氧化碳 | B. | 10g氢气和10g氧气 | ||
| C. | 22.4mL氢气(标况)和0.1mol氮气 | D. | 22g二氧化碳和16.8L溴单质(Br2) |
1.下列离子方程式正确的是( )
| A. | 稀硫酸与氢氧化钡溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 将大理石投入到足量盐酸中:CO32-+2H+═CO2↑+H2O | |
| C. | 将Cl2与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 碳酸钠溶液显碱性:CO32-+H2O?HCO3-+OH- |
8.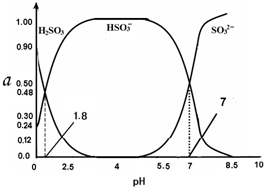 常温下 0.1mol•L-1 亚硫酸溶液中H2SO3、HSO3-、SO32- 三者中所占物质的量分数(α)随pH 变化的关系如图所示.下列表述 正确的是( )
常温下 0.1mol•L-1 亚硫酸溶液中H2SO3、HSO3-、SO32- 三者中所占物质的量分数(α)随pH 变化的关系如图所示.下列表述 正确的是( )
 常温下 0.1mol•L-1 亚硫酸溶液中H2SO3、HSO3-、SO32- 三者中所占物质的量分数(α)随pH 变化的关系如图所示.下列表述 正确的是( )
常温下 0.1mol•L-1 亚硫酸溶液中H2SO3、HSO3-、SO32- 三者中所占物质的量分数(α)随pH 变化的关系如图所示.下列表述 正确的是( )| A. | H2SO3?2H++SO32- K=10-5.2 | |
| B. | 在0.1mol•L H2SO3溶液中,存在:c2(H+)=c(H+)•c(HSO3-)+2c(H+)•c(SO32-)+Kw | |
| C. | 在pH=2.5 溶液中:c(H2SO3)>c(HSO3-)>c(H+)>c(OH-) | |
| D. | 向pH 为 8.5 的上述体系中通入极少量 Cl2 的过程中,溶液中c(HSO3-)和c(SO32-)均减小 |
6.对盐的组成叙述正确的是( )
| A. | 都含有原子团 | B. | 都含有金属元素 | ||
| C. | 都不含氢元素 | D. | 都含有非金属元素 |
