题目内容
17.将24g可能含Na、Mg、Al、Fe的合金投入稀HCl中放出氢气的质量为2g,则此合金中一定含( )| A. | Na | B. | Mg | C. | Al | D. | Fe |
分析 2g氢气的物质的量为:$\frac{2g}{2g/mol}$=1mol,假设金属都是+2价,则金属的物质的量为1mol,混合金属的平均摩尔质量为:$\frac{24g}{1mol}$=24g/mol,Na为+2价时的摩尔质量为23g/mol×2=46g/mol,Mg、Fe与稀盐酸反应都表现+2价,Al为+2价时的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,据此进行判断合金组成.
解答 解:2g氢气的物质的量为:$\frac{2g}{2g/mol}$=1mol,假设金属都是+2价,则金属的物质的量为1mol,混合金属的平均摩尔质量为:$\frac{24g}{1mol}$=24g/mol,
Na为+2价时的摩尔质量为23g/mol×2=46g/mol,
Mg的摩尔质量为24g/mol,
Fe与稀盐酸反应都表现+2价,其摩尔质量为56g/mol,
Al为+2价时的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,
根据分析可知,Na、Fe的+2价摩尔质量都大于24g/mol,Mg的摩尔质量=24g/mol,只有Al为+2价时的摩尔质量<24g/mol,
所以若满足合金平均摩尔质量为24g/mol,合金中一定含有Al,
故选C.
点评 本题考查了化学方程式的计算,题目难度不大,明确发生反应原理为解答关键,注意掌握平均值发在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
7.下列表示物质形成过程的电子式正确的是( )
| A. | 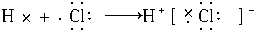 | |
| B. | 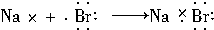 | |
| C. | 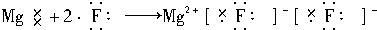 | |
| D. | 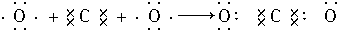 |
8.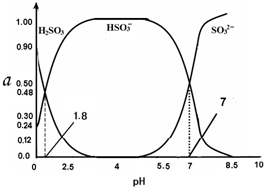 常温下 0.1mol•L-1 亚硫酸溶液中H2SO3、HSO3-、SO32- 三者中所占物质的量分数(α)随pH 变化的关系如图所示.下列表述 正确的是( )
常温下 0.1mol•L-1 亚硫酸溶液中H2SO3、HSO3-、SO32- 三者中所占物质的量分数(α)随pH 变化的关系如图所示.下列表述 正确的是( )
 常温下 0.1mol•L-1 亚硫酸溶液中H2SO3、HSO3-、SO32- 三者中所占物质的量分数(α)随pH 变化的关系如图所示.下列表述 正确的是( )
常温下 0.1mol•L-1 亚硫酸溶液中H2SO3、HSO3-、SO32- 三者中所占物质的量分数(α)随pH 变化的关系如图所示.下列表述 正确的是( )| A. | H2SO3?2H++SO32- K=10-5.2 | |
| B. | 在0.1mol•L H2SO3溶液中,存在:c2(H+)=c(H+)•c(HSO3-)+2c(H+)•c(SO32-)+Kw | |
| C. | 在pH=2.5 溶液中:c(H2SO3)>c(HSO3-)>c(H+)>c(OH-) | |
| D. | 向pH 为 8.5 的上述体系中通入极少量 Cl2 的过程中,溶液中c(HSO3-)和c(SO32-)均减小 |
12.将51.2g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O、NO+NO2+2NaOH=2NaNO2+H2O.则生成的盐溶液中NaNO2的物质的量为( )
| A. | 0.2 mol | B. | 0.4 mol | C. | 0.6 mol | D. | 0.8 mol |
2.下列关于有机物的说法错误的是( )
| A. | 乙烯和苯均能发生加成反应 | |
| B. | 石油干馏可得到汽油、煤油等 | |
| C. | 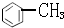 的一溴代物和 的一溴代物和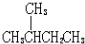 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) | |
| D. | 乙酸乙酯、油脂、淀粉均能发生水解反应 |
9.设NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A. | NA个氮气分子与3NA个氢气分子恰好生成2NA个氨气分子 | |
| B. | 在1L0.1mol/L的AICI3溶液中含有0.1NA个AI3+ | |
| C. | 常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数为2NA | |
| D. | 5.6g的铁与足量的稀硝酸反应转移的电子数是0.3NA |
6.对盐的组成叙述正确的是( )
| A. | 都含有原子团 | B. | 都含有金属元素 | ||
| C. | 都不含氢元素 | D. | 都含有非金属元素 |
7.金属M与AgNO3溶液反应的化学方程式为M+2AgNO3=M(NO3)2+2Ag.若M是铜,则下列说法错误的是( )
| A. | M的金属活动性比Ag强 | B. | 反应后溶液的质量增加 | ||
| C. | 金属M不可能变换成铝 | D. | 固体物质的质量增加了 |