题目内容
下列电离方程式中,正确的是( )
| A、Al2(SO4)3═2Al3++3SO42- |
| B、NaHCO3═Na++H++CO32- |
| C、CH3COOH═CH3COO-+H+ |
| D、Na2CO3═Na2++CO32- |
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:强电解质在水溶液里完全电离生成阴阳离子,电离方程式写“=”,弱电解质在水溶液里部分电离,电离方程式写“?”,书写时要遵循原子守恒、电荷守恒,以此解答该题.
解答:
解:A.Al2(SO4)3为强电解质,电离方程式为Al2(SO4)3═2Al3++3SO42-,故A正确;
B.NaHCO3电离出钠离子和HCO3-,电离方程式为NaHCO3═Na++HCO3-,故B错误;
C.CH3COOH为弱酸,部分电离,电离方程式为CH3COOH?CH3COO-+H+,故C错误;
D.离子符合错误,电离方程式应为Na2CO3═2Na++CO32-,故D错误.
故选A.
B.NaHCO3电离出钠离子和HCO3-,电离方程式为NaHCO3═Na++HCO3-,故B错误;
C.CH3COOH为弱酸,部分电离,电离方程式为CH3COOH?CH3COO-+H+,故C错误;
D.离子符合错误,电离方程式应为Na2CO3═2Na++CO32-,故D错误.
故选A.
点评:本题考查了电离方程式的书写,为高频考点,明确电解质的强弱及电离方程式的书写规则是解本题关键,注意原子团不能拆开,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
鉴别纯碱,石灰石,芒硝、石膏四种白色固体物质,下列试剂中应该选用( )
| A、NaOH溶液 |
| B、HNO3溶液 |
| C、水和盐酸 |
| D、BaCl2和HNO3溶液 |
某强氧化剂RO3-中R元素能被还原成较低的价态,如果还原2.4×10-2molRO3-需要6×10-2molNa2SO3(Na2SO3转化成Na2SO4),则反应后R元素的价态是( )
| A、0 | B、+1 | C、+3 | D、+4 |
已知某溶液中仅存在OH-、H+、NH4+、Cl-四种离子,其浓度大小有如下关系,其中一定不正确的是( )
| A、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
| B、C(C1-)=C(NH4+),且C(H+)═C(OH-) |
| C、C(NH4+)<C(Cl-)<C(H+)<C(OH-) |
| D、C(OH-)<C(NH4+)<C(H+)<C(Cl-) |
高温下,某反应达到平衡,平衡常数K=
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| A、该反应的焓变为正值 | |||
| B、恒温恒容下,增大压强,H2浓度一定减小 | |||
| C、升高温度,逆反应速率减小 | |||
D、该反应的化学方程式为CO+H2O
|
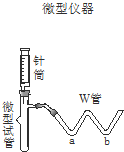 现有一瓶实验室放置已久的可能被氧化的Na2SO3固体,为了研究它的组成,请你参与同学们进行的如下探究活动:
现有一瓶实验室放置已久的可能被氧化的Na2SO3固体,为了研究它的组成,请你参与同学们进行的如下探究活动: