题目内容
17.设阿伏加德罗常数的值为NA,下列叙述正确的是( )| A. | 标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2NA | |
| B. | 0.1mol${\;}_{35}^{81}$Br原子中含中子数为3.5NA | |
| C. | 6.0g SiO2晶体中含有的硅氧键数目为0.4NA | |
| D. | 7.8g过氧化钠中所含有的阴离子数为0.2NA |
分析 A、氦气为单原子分子;
B、${\;}_{35}^{81}$Br原子中含46个中子;
C、求出二氧化硅的物质的量,然后根据1mol二氧化硅中含4mol硅氧键来分析;
D、求出过氧化钠的物质的量,然后根据1mol过氧化钠中含2mol钠离子和1mol过氧根来分析.
解答 解:A、氦气为单原子分子,故标况下22.4L氦气的物质的量为1mol,含NA个原子,故A错误;
B、${\;}_{35}^{81}$Br原子中含46个中子,故0.1mol中含4.6NA个中子,故B错误;
C、6.0g二氧化硅的物质的量为0.1mol,而1mol二氧化硅中含4mol硅氧键,故0.1mol二氧化硅中含0.4NA个硅氧键,故C正确;
D、7.8g过氧化钠的物质的量为0.1mol,而1mol过氧化钠中含2mol钠离子和1mol过氧根,故0.1mol过氧化钠中含0.1NA个阴离子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.化学与生活密切相关,下列有关说法中不正确的是( )
| A. | 工业上常利用油脂的碱性水解制取肥皂 | |
| B. | 雾、鸡蛋清水溶液、水与乙醇的混合液均具有丁达尔效应 | |
| C. | 蔬菜汁饼干易氧化变质:建议包装饼干时,加入一小包铁粉作抗氧化剂和吸水剂并密封 | |
| D. | 浸泡过高锰酸钾溶液的硅藻士可以吸收乙烯,所以可用此物保鲜水果 |
8.下列反应所得有机产物只有一种的是( )
| A. | 等体积的甲烷与氯气在光照条件下的取代反应 | |
| B. | 丙烯与氯化氢的加成反应 | |
| C. | 2-丙醇在浓硫酸作用下的消去反应 | |
| D. | 乙炔与溴水的加成反应 |
5.下列有关说法正确的是( )
| A. | 实验室制氢气,为了加快反应速率,可向稀 H2SO4 中滴加少量 Cu(NO3)2 溶液 | |
| B. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,平衡时氢气转化率增大 | |
| C. | 吸热反应“TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 | |
| D. | 在稀AgNO3溶液中加入过量 NaCl溶液,产生白色沉淀,再加入少量 Na2S溶液,出现黑色沉淀,则加入Na2S溶液后 c(Ag+) 更小了 |
12.下列实验操作正确的是( )
| A. | 用带橡皮塞的棕色细口瓶盛放浓硝酸 | |
| B. | 滴定管经蒸馏水润洗后,即可注入标准液进行滴定 | |
| C. | 用干燥清洁的玻璃棒蘸取某溶液点在pH试纸中部,跟标准比色卡比较来测定该溶液的pH | |
| D. | 配制溶液时加水超过容量瓶的标线,用滴管把多余的液体吸出 |
2.2008年北京奥运会“祥云”奥运火炬所用环保型燃料丙烷(C3H8),悉尼奥运会所用火炬燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为:2221.5kJ•mol-1;正丁烷的燃烧热为:2878kJ•mol-1;异丁烷的燃烧热为:2869kJ•mol-1.下列有关说法正确的是( )
| A. | 丙烷燃烧的热化学方程式可表示为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5 kJ•mol-1 | |
| B. | 正丁烷燃烧的热化学方程式可表示为:2C4H10(g)+18O2(g)=8CO2(g)+10H2O(l);△H=-2878 kJ•mol-1 | |
| C. | 正丁烷转化为异丁烷的过程是一个放热过程 | |
| D. | 正丁烷比异丁烷稳定 |
9.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 2 L 0.5 mol/L硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 0.1 mol丙烯酸中含有双键的数目为0.1NA | |
| D. | 3mol单质Fe完全转变为Fe3O4失去8NA个电子 |
7.同分异构现象是造成有机物数目繁多的原因之一.下列物质互为同分异构体的是( )


| A. | Ⅰ和Ⅱ | B. | Ⅱ和Ⅲ | C. | Ⅲ和Ⅳ | D. | Ⅰ和Ⅳ |
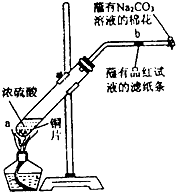 在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中.塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花.给试管加热,观察现象.当试管中的液体逐渐透明时,停止加热.回答下列问题:
在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中.塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花.给试管加热,观察现象.当试管中的液体逐渐透明时,停止加热.回答下列问题: