题目内容
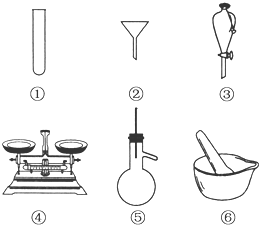 (1)下列仪器常用于物质分离的是
(1)下列仪器常用于物质分离的是(2)配制250mL 4.0mol?L-1 NaOH溶液的实验步骤:
a.计算需要氢氧化钠固体的质量.
b.称量氢氧化钠固体.
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶.
d.用适量蒸馏水溶解称量好的氢氧化钠固体,冷却.
e.盖好瓶塞,反复上下颠倒,摇匀.
f.继续向容量瓶中加蒸馏水至刻度线下1cm~2cm时,改用胶头滴管加蒸馏水至凹液面与刻度线相切.
①所需称量的氢氧化钠固体的质量是
②上述步骤的正确操作顺序是(填序号)
③上述实验需要的玻璃仪器除胶头滴管、烧杯外还有
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)常用的分离操作有过滤、蒸发、蒸馏、萃取、分液等,由图可知,①为量筒,②为漏斗,③为蒸馏烧瓶,④为托盘天平,⑤为蒸馏烧瓶,⑥研钵,结合仪器的用途来解答;
(2)①根据n=CV,m=nM计算氢氧化钠的质量;
②配制250mL 4.0mol?L-1NaOH溶液,应按照计算、称量、溶解、移液、洗涤、定容、摇匀的步骤;
③根据操作的步骤确定所需仪器.
(2)①根据n=CV,m=nM计算氢氧化钠的质量;
②配制250mL 4.0mol?L-1NaOH溶液,应按照计算、称量、溶解、移液、洗涤、定容、摇匀的步骤;
③根据操作的步骤确定所需仪器.
解答:
解:(1)①量筒常用于量取液体的体积,不能用于物质的分离;
②普通漏斗常用于过滤,可用来分离固液混合物;
③分液漏斗用来分液,可以分离互不溶解的两种液体;
④托盘天平用来称量固体的质量,不能用于分离物质;
⑤蒸馏烧瓶常用于分离沸点不同的液体混合物;
⑥研钵用于研磨固体物质或进行粉末状固体的混和,不能用于物质的分离;
所以用来分离的仪器有②③⑤,
故答案为:②③⑤;
(2)①配制250mL 4.0mol?L-1 NaOH溶液,需要称取氢氧化钠的物质的量n(NaOH)=0.25L×4mol/L=1mol,m(NaOH)=1mol×40g/mol=40.0g,
故答案为:40.0g;
②配制250mL 4.0mol?L-1NaOH溶液,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,则正确的顺序为a b d c f e,
故答案为:a b d c f e;
③配制250mL 4.0mol?L-1NaOH溶液,需要的仪器有托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管,所以还需要的玻璃仪器为:玻璃棒;250 mL容量瓶;
故答案为:玻璃棒、250 mL容量瓶.
②普通漏斗常用于过滤,可用来分离固液混合物;
③分液漏斗用来分液,可以分离互不溶解的两种液体;
④托盘天平用来称量固体的质量,不能用于分离物质;
⑤蒸馏烧瓶常用于分离沸点不同的液体混合物;
⑥研钵用于研磨固体物质或进行粉末状固体的混和,不能用于物质的分离;
所以用来分离的仪器有②③⑤,
故答案为:②③⑤;
(2)①配制250mL 4.0mol?L-1 NaOH溶液,需要称取氢氧化钠的物质的量n(NaOH)=0.25L×4mol/L=1mol,m(NaOH)=1mol×40g/mol=40.0g,
故答案为:40.0g;
②配制250mL 4.0mol?L-1NaOH溶液,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,则正确的顺序为a b d c f e,
故答案为:a b d c f e;
③配制250mL 4.0mol?L-1NaOH溶液,需要的仪器有托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管,所以还需要的玻璃仪器为:玻璃棒;250 mL容量瓶;
故答案为:玻璃棒、250 mL容量瓶.
点评:本题考查了物质分离的方法和仪器、配制一定物质的量浓度溶液的步骤和需要的仪器,题目难度不大,熟悉仪器的用途和配制过程是解题关键.

练习册系列答案
相关题目
下列各组离子在溶液中可以大量共存的是( )
| A、H+、SO32-、S2-、K+ |
| B、Na+、K+、S2-、SO42- |
| C、HSO3-、Cl-、OH-、Ba2+ |
| D、Cu2+、Cl-、OH-、K+ |

