题目内容
碘化钠和氯化钠的混合物10g,跟足量Cl2反应后,经加热、烘干最后得固体6.64g,求混合物中NaCl的质量分数.
考点:化学方程式的有关计算,氯、溴、碘及其化合物的综合应用
专题:计算题,卤族元素
分析:生成的I2在加热烘干时升华,最后得6.64g固体为NaCl,计算反应前后固体质量差,利用差量法计算NaI的质量,进而计算混合物中NaCl的质量,再计算混合物中氯化钠的质量分数.
解答:
解:生成的I2在加热烘干时升华,最后得6.64g固体为NaCl,则反应后固体质量减少10g-6.64g=3.36g,则:
2NaI+Cl2=2NaCl+I2 固体质量减少
300 183
x 3.36g
x=
=5.5g,
故原混合物中NaCl的质量为10g=5.5g=4.5g,
混合物中NaCl的质量分数=
×100%=45%,
答:混合物中氯化钠的质量分数为45%.
2NaI+Cl2=2NaCl+I2 固体质量减少
300 183
x 3.36g
x=
| 3.36g×300 |
| 183 |
故原混合物中NaCl的质量为10g=5.5g=4.5g,
混合物中NaCl的质量分数=
| 4.5g |
| 10g |
答:混合物中氯化钠的质量分数为45%.
点评:本题考查混合物计算,难度不大,明确固体减少原因是关键,注意利用差量法解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体c呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )
在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体c呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )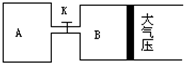 如图所示,当关闭K时,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)?Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
如图所示,当关闭K时,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)?Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答: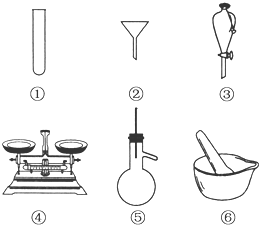 (1)下列仪器常用于物质分离的是
(1)下列仪器常用于物质分离的是