题目内容
下列各组离子在溶液中可以大量共存的是( )
| A、H+、SO32-、S2-、K+ |
| B、Na+、K+、S2-、SO42- |
| C、HSO3-、Cl-、OH-、Ba2+ |
| D、Cu2+、Cl-、OH-、K+ |
考点:离子共存问题
专题:离子反应专题
分析:A.氢离子与亚硫酸根离子、硫离子之间反应反应生成硫单质;
B.Na+、K+、S2-、SO42-离子之间不满足离子反应发生条件;
C.亚硫酸氢根离子与氢氧根离子、钡离子反应生成亚硫酸钡沉淀;
D.铜离子与氢氧根离子反应生成氢氧化铜沉淀.
B.Na+、K+、S2-、SO42-离子之间不满足离子反应发生条件;
C.亚硫酸氢根离子与氢氧根离子、钡离子反应生成亚硫酸钡沉淀;
D.铜离子与氢氧根离子反应生成氢氧化铜沉淀.
解答:
解:A.H+与SO32-、S2-之间反应生成硫单质,在溶液中不能大量共存,故A错误;
B.Na+、K+、S2-、SO42-之间不发生反应,在溶液中能够大量共存,故B正确;
C.HSO3-与OH-、Ba2+之间反应生成亚硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.Cu2+、OH-之间反应生成难溶物氢氧化铜,在溶液中不能大量共存,故D错误;
故选B.
B.Na+、K+、S2-、SO42-之间不发生反应,在溶液中能够大量共存,故B正确;
C.HSO3-与OH-、Ba2+之间反应生成亚硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.Cu2+、OH-之间反应生成难溶物氢氧化铜,在溶液中不能大量共存,故D错误;
故选B.
点评:本题考查离子共存的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等; 试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式正确的是( )
| A、醋酸铵和盐酸反应 CH3COONH4+H+═CH3COOH+NH4+ |
| B、氢氧化钡溶液和硫酸铜溶液反应 Ba2++SO42-═BaSO4↓ |
| C、钠与水反应 Na+2H2O═Na++OH-+H2↑ |
| D、碳酸氢钠溶液与NaOH溶液反应:HCO3-+OH-=CO32-+H2O |
下列叙述正确的是( )
| A、鸡蛋白溶液中,加入浓的硫酸铵溶液有沉淀析出,加入水后沉淀不溶解 |
| B、蛋白质水解的最后产物是氨基酸 |
| C、重金属盐使蛋白质变性,所以吞食“钡餐”会引起中毒 |
| D、人体中的氨基酸都不能自身合成 |
某溶液中含有CH3COO-、SO
、SO
、HCO
、CO
五种离子,将过量的Na2O2固体加入其中后,仍能大量存在的离子是( )
2- 4 |
2- 3 |
- 3 |
2- 3 |
A、CH3COO-、SO
| ||||||
B、SO
| ||||||
C、SO
| ||||||
D、CH3COO-、SO
|
将Na2CO3?10H2O和NaHCO3的混合物11.94g,溶于水配制成200mL溶液,测得Na+浓度c(Na+)=0.5mol/L.若将11.94g该混合物加热至质量不再改变时,得到的固体物质的质量为( )
| A、3.1g | B、5.3g |
| C、9.0g | D、11.0g |
足量的MnO2与33.3mL 12mol/L浓盐酸反应,同0.1mol MnO2与足量的浓盐酸反应产生的氯气两者相比( )
| A、前者多 | B、后者多 |
| C、一样多 | D、无法确定 |
随着2011年6月30日西气东输二线全线建成投产,预计年内西气东输的输气能力将增加百亿立方米.这里的“气”指的是“天然气”,主要成分是甲烷.下列关于甲烷的说法正确的是( )
| A、实验室可以用排水法收集甲烷 |
| B、只有纯净甲烷在空气中安静燃烧 |
| C、甲烷与氯水发生取代反应 |
| D、甲烷在空气中燃烧只生成二氧化碳和水 |
 在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体c呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )
在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体c呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )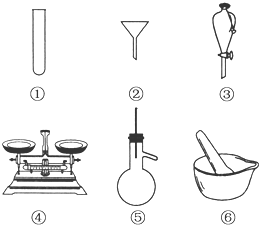 (1)下列仪器常用于物质分离的是
(1)下列仪器常用于物质分离的是