题目内容
下列物质的分类全部正确的是( )
| A、NO2-酸性氧化物 Na2O2-碱性氧化物 Al2O3-两性氧化物 |
| B、汽油-混合物 胆矾-纯净物 金刚石-单质 |
| C、纯碱-碱 硫化氢-酸 小苏打-酸式盐 |
| D、液氯-非电解质 硫酸钡-强电解质 醋酸-弱电解质 |
考点:酸、碱、盐、氧化物的概念及其相互联系,混合物和纯净物,强电解质和弱电解质的概念
专题:物质的分类专题
分析:A.酸性氧化物是和碱反应生成盐和水的氧化物,碱性氧化物是和酸反应生成盐和水的氧化物,发生的都是复分解反应;
B.根据单质、纯净物、混合物的定义和分类判断;
C.根据酸碱盐的定义判断;
D.根据电解质、非电解质等定义判断.
B.根据单质、纯净物、混合物的定义和分类判断;
C.根据酸碱盐的定义判断;
D.根据电解质、非电解质等定义判断.
解答:
解:A.依据酸性氧化物和碱性氧化物的概念分析判断,NO2不是酸性氧化物、Na2O2不属于碱性氧化物,故A错误;
B.汽油-混合物、胆矾-纯净物、金刚石-单质,故B正确;
C.纯碱是碳酸钠,属于盐不是碱,故C错误;
D.非电解质属于化合物,液氯是单质,既不是电解质也不是非电解质,故D错误;
故选B.
B.汽油-混合物、胆矾-纯净物、金刚石-单质,故B正确;
C.纯碱是碳酸钠,属于盐不是碱,故C错误;
D.非电解质属于化合物,液氯是单质,既不是电解质也不是非电解质,故D错误;
故选B.
点评:本题考查物质的分类,难度不大,注意掌握相关的概念是解题的关键.

练习册系列答案
相关题目
高铁电池是一种新型可充电电池,电解质溶液为KOH,放电时的总反应式为:3Zn+2K2FeO4+8H2O?3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
| A、充电时阳极反应式为:3Zn(OH)2+6e-═3Zn+6OH- |
| B、放电时OH-向正极移动 |
| C、充电时每转移3mol电子,阳极有1mol Fe(OH)3被还原 |
| D、放电时负极反应为:3Zn-6e-+6OH-═3Zn(OH)2 |
用下列实验装置进行相应实验,能达到实验目的是( )
A、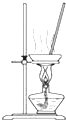 如图所示装置,蒸干AlCl3饱和溶液制备AlCl3晶体 |
B、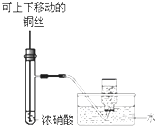 如图所示装置,制备并收集少量NO2气体 |
C、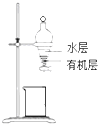 如图所示装置,分离CCl4萃取I2水后的有机层和水层 |
D、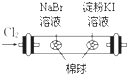 如图所示装置,可以证明氧化性:Cl2>Br2>I2 |
已知电离平衡常数:H2CO3>HClO>HCO3-,氧化性:HClO>Cl2>Br2>Fe3+>I2.下列有关离子反应或离子方程式的叙述中,正确的是( )
| A、向NaClO溶液中通入少量二氧化碳的离子方程式:2ClO-+CO2+H2O═2HClO+CO32- |
| B、向溴水中加入足量氯化亚铁溶液能使溴水变成无色 |
| C、能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存 |
| D、向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl- |
下列反应的离子方程式不正确的是( )
| A、铁和稀盐酸反应:Fe+2H+═Fe2++H2↑ |
| B、碳酸钙溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O |
| C、硫酸溶液中加入碳酸氢钠溶液:H++HCO3-═CO2↑+H2O |
| D、在氢氧化钾的稀溶液中通过量的二氧化碳气体:CO2+OH-═HCO3- |
在相同条件下,A容器中盛有Cl2,B容器中盛有NH3,若两容器中所含的原子数相等,则A容器与B容器的体积比为( )
| A、2:1 | B、1:3 |
| C、1:2 | D、2:3 |
下列各组指定原子序数的元素,能形成A2B3型化合物的是( )
| A、6和8 | B、11和9 |
| C、12和17 | D、13和8 |