题目内容
14.配制一定物质的量浓度的某溶液,下列情况会使溶液浓度偏低的是( )| A. | 未冷却即转移、定容 | B. | 溶液转移后,未洗涤烧杯和玻璃棒 | ||
| C. | 定容时俯视刻度线 | D. | 容量瓶中原有少量蒸馏水 |
分析 由c=$\frac{n}{V}$可知,不当操作使n偏小或V偏大均使溶液浓度偏低,以此来解答.
解答 解:A.未冷却即转移、定容,V偏小,则溶液浓度偏大,故A不选;
B.溶液转移后,未洗涤烧杯和玻璃棒,n偏小,使溶液浓度偏低,故B选;
C.定容时俯视刻度线,V偏小,则溶液浓度偏大,故C不选;
D.容量瓶中原有少量蒸馏水,对实验无影响,故D不选;
故选B.
点评 本题考查配制一定浓度的溶液,为高频考点,把握浓度与物质的量、体积的关系及实验操作为解答的关键,侧重分析与实验能力的考查,注意结合公式分析误差,题目难度不大.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
5.T℃时,将A和B各0.32mol充入恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)△H=-a kJ•mol-1(a>0),反应过程中测定的数据如表,下列说法正确的是( )
| t/min | 0 | 2 | 4 | 7 | 9 |
| n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
| A. | 若起始时向容器中充入0.64 mol C,则达平衡时吸收的热量为0.12a kJ | |
| B. | 恒温,如果压缩容器体积,B的浓度和体积分数均不变 | |
| C. | 若起始时向容器中充入 0.64 mol A 和 0.64 mol B,则达平衡时 n(C)<0.48 mol | |
| D. | 恒温、恒容,向平衡体系中再充入0.32 mol A,再次平衡时,B的转化率增大 |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| B. | 常温常压下,46gNO2和N2O4的混合气体中含有的原子总数为3NA | |
| C. | 78gNa2S和Na2O2的混合物中阳离子和阴离子的总数为3.5NA | |
| D. | 标准状况下,2.24 L乙炔中含有共价键数目为0.5 NA |
6.已知某物质的物质的量,下列物理量中一定能够计算出值的是( )
| A. | 体积 | B. | 质量 | C. | 密度 | D. | 粒子数 |
3.下列有关化学实验安全问题的叙述中不正确的是( )
| A. | 少量的浓硫酸或浓NaOH沾到皮肤上,应用大量的水反复冲洗,再涂抹相应的药品 | |
| B. | 氢气还原氧化铜,一般先预热氧化铜,然后再通入氢气 | |
| C. | 浓硝酸需用细口棕色试剂瓶密封保存 | |
| D. | 实验室制备有毒气体应在通风橱中进行,且必须对尾气进行吸收或处理 |
4.下列物质属于电解质的是( )
| A. | SO2 | B. | Cu | C. | 蔗糖 | D. | 固体NaCl |
 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用图1表示:
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用图1表示: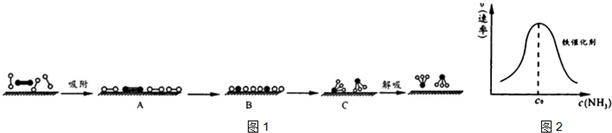
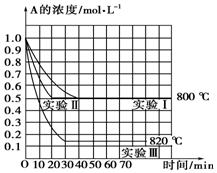 在一恒容密闭容器中发生某化学反应2A(g)?B(g)+C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ在800℃,实验Ⅲ在820℃,B、C的起始浓度都为0,反应物A的浓度(mol•L-1)随时间(min)的变化如图所示,请回答:
在一恒容密闭容器中发生某化学反应2A(g)?B(g)+C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ在800℃,实验Ⅲ在820℃,B、C的起始浓度都为0,反应物A的浓度(mol•L-1)随时间(min)的变化如图所示,请回答: