题目内容
20.下列说法中,正确的是( )①镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀;
②钢铁表面常易锈蚀生成Fe2O3•nH2O;
③锌和铁构成原电池时,铁作负极;
④铅蓄电池中铅作负极,PbO2作正极,两极浸到H2SO4中.
| A. | 只有②④ | B. | 只有①③ | C. | ①②③ | D. | ①②③④ |
分析 ①在原电池中,活泼金属做负极,负极金属更易腐蚀,正极金属被保护;
②铁锈的主要成分为Fe2O3•nH2O;
③锌比铁活泼;
④铅蓄电池中,铅板做负极,PbO2做正极.
解答 解:①白铁(镀锌的铁)中,镀层破损后,Zn为负极,被腐蚀的是Zn,Fe被保护,马口铁(镀锡的铁)中,Fe为负极,被腐蚀的是Fe,Zn被保护,所以镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)铁更耐腐蚀,故①错误;
②铁锈的主要成分为Fe2O3•nH2O,是由铁的吸氧腐蚀形成的,故②正确;
③锌比铁活泼,故锌做负极,故③错误;
④铅蓄电池中,铅板做负极,PbO2做正极,两极浸到H2SO4中,故④正确.
故选A.
点评 本题是一道综合知识题目,考查学生对原电池原理的应用知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
10.下列分子只表示一种物质的是( )
| A. | C3H7Cl | B. | C3H8 | C. | C4H10 | D. | C2H6O |
8.500mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到11.2L气体(标准状况).下列说法正确的是( )
| A. | 原混合溶液中c(K+)为3mol/L | B. | 上述电解过程中共转移4 mol电子 | ||
| C. | 电解得到的Cu的物质的量为0.5mol | D. | 电解后溶液上c(H+)为4 mol/L |
15.具有手性碳原子的物质具有旋光性,存在对映异构体,下列化合物中存在对映异构体的是( )
| A. | CH3CHClCH2CH3 | B. | CH3CH3 | C. | 甲烷 | D. | CH3COOH |
12.2015年巴黎气候变化大会召开,旨在保护环境造福人类.下列说法不正确的是( )
| A. | 扩大铅蓄电池、汞锌锰干电池的生产,满足消费需求 | |
| B. | 采用碳捕集和储存技术,逐步实现二氧化碳的零排放 | |
| C. | 对工业废水、生活污水净化处理,减少污染物的排放 | |
| D. | 催化处理汽车尾气,减轻氮氧化物污染和光化学烟雾 |
9.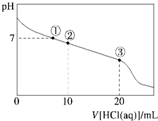 常温下,向20.00mL 0.100mol•L-1 CH3COONa溶液中逐滴加入0.100 0mol•L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发).下列说法正确的( )
常温下,向20.00mL 0.100mol•L-1 CH3COONa溶液中逐滴加入0.100 0mol•L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发).下列说法正确的( )
 常温下,向20.00mL 0.100mol•L-1 CH3COONa溶液中逐滴加入0.100 0mol•L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发).下列说法正确的( )
常温下,向20.00mL 0.100mol•L-1 CH3COONa溶液中逐滴加入0.100 0mol•L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发).下列说法正确的( )| A. | 点①所示溶液中:c(CH3COOH)=c(Cl-)>c(OH-)=c(H+) | |
| B. | 点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) | |
| C. | 点③所示溶液中:c(CH3COOH)>c(Na+)>c(H+)>c(CH3COO-) | |
| D. | 整个过程中可能出现:c(H+)+c(Na+)═c(CH3COOH)+c(CH3COO-) |
10.如图是某太阳光伏电池示意图.则有关叙述正确的是( )


| A. | 光伏电池是将化学能转变为电能 | |
| B. | 光伏电池是将太阳能转变为热能 | |
| C. | 电流从b流向a | |
| D. | 图中P型半导体为负极,N型半导体为正极 |
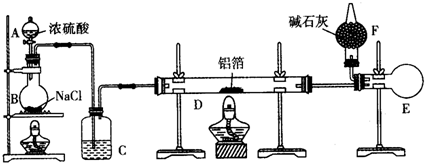
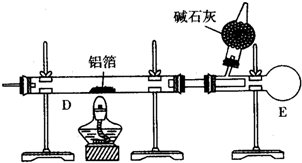
 A是一种重要的化工原料,用来衡量一个国家的石油化工发展水平,相同条件下存在如下转化关系(部分反应物、反应条件和产物已省略),其中E为具有果香气味的物质,F是高聚物.
A是一种重要的化工原料,用来衡量一个国家的石油化工发展水平,相同条件下存在如下转化关系(部分反应物、反应条件和产物已省略),其中E为具有果香气味的物质,F是高聚物.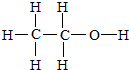 ;写出其官能团的电子式
;写出其官能团的电子式 ,1个该官能团含有9个电子,氢氧根与其组成元素相同,电子式为
,1个该官能团含有9个电子,氢氧根与其组成元素相同,电子式为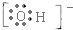 ,含有有10个电子;高聚物F是常用的塑料之一,它的链节可表示为-CH2CH2-.
,含有有10个电子;高聚物F是常用的塑料之一,它的链节可表示为-CH2CH2-.