题目内容
2.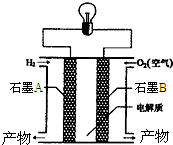 氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | B电极上发生氧化反应 | |
| B. | A电极是负极 | |
| C. | 该电池的总反应为2H2+O2=2H2O | |
| D. | 外电路中电子由A电极通过导线流向B电极 |
分析 A.氢氧燃料在电极上反应的分别是氢气和氧气,通氢气一极发生氧化反应;
B.燃料电池中,负极上通入燃料,发生氧化反应,正极上通入氧气,发生还原反应;
C.该电池反应式和氢气燃烧方程式相似;
D.原电池中,电子从负极沿导线流向正极,电流方向与电子流向相反.
解答 解:A.氢氧燃料在电极上反应的分别是氢气和氧气,通氢气一极发生氧化反应,所以A极发生氧化反应,故A错误;
B、A是负极,故B正确;
C、该电池反应式和氢气燃烧方程式相似,所以其电池反应式为2H2+O2═2H2O,故C正确;
D、电子从负极A沿导线流向正极B,电流方向与电子流向相反,故D正确;
故选A.
点评 本题考查了化学电源新型电池,根据得失电子确定正负极,再结合电子移动方向、电池反应式来分析解答,难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目
12.现在人们已能合成自然界并不存在的许多性能优良的有机高分子材料,如由氯乙烯合成聚氯乙烯,则适合于合成聚氯乙烯的原料是( )
| A. | CH4、Cl2 | B. | CH3CH3、HCl | C. | CH≡CH、HCl | D. | CH2=CH2、HCl |
13.向溶液X中持续通入气体Y,会产生“浑浊→澄清”现象的是( )
| A. | X:氯化铝溶液,Y:氨气 | |
| B. | X:硅酸钠溶液,Y:二氧化硫 | |
| C. | X:氢氧化钡溶液,Y:一氧化碳 | |
| D. | X:四羟基合铝酸钠溶液,Y:二氧化氮 |
10.用布氏漏斗和吸滤瓶接抽水泵过滤沉淀后,正确的操作是( )
| A. | 先关水龙头,拔下抽滤瓶上的橡皮管,再取下布氏漏斗 | |
| B. | 先取下布氏漏斗,再关上水龙头 | |
| C. | 先将沉淀和滤纸一起取出,再关上水龙头 | |
| D. | 先拔下抽滤瓶上的橡皮管,关上水龙头,再取下布氏漏斗 |
17.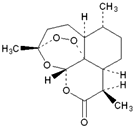 2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )
2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )
 2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )
2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )| A. | 难溶于水,易溶于乙醚 | B. | 在热的NaOH溶液中可发生水解反应 | ||
| C. | 一定条件下能与氯气发生取代反应 | D. | 化学式为C15H21O5 |
14.在一定温度下的定容密闭容器中,当下列物理量不再变化时,表明反应A(s)+2B(g)?C(g)+D(g)已经到达平衡的是( )
| A. | 混合气体的压强 | |
| B. | 混合气体的密度 | |
| C. | 当B、C、D三种物质,它们的物质的量nB:nC:nD=2:1:1 | |
| D. | 混合气体的总物质的量 |
11.酸碱质子理论的要点是:凡能给出质子(即H+)的分子或离子都是酸;凡能接受质子的分子或离子都是碱.按此观点,下列微粒既属于酸又属于碱的是( )
①H2O ②CO32-③Al3+ ④CH3COOH ⑤NH4+ ⑥HCO3-.
①H2O ②CO32-③Al3+ ④CH3COOH ⑤NH4+ ⑥HCO3-.
| A. | ②③ | B. | ①⑥ | C. | ④⑥ | D. | ⑤⑥ |
12.取m g AgNO3固体粉末充分加热,得到a L气体和b g固体,将气体用足量的水吸收,剩余气体的体积为c L(气体体积均为同温同压下测定),下列结论一定正确的是( )
| A. | aL气体的平均相对分子质数为41.3 | |
| B. | aL气体被水吸收时转移电子的物质的量为($\frac{2m}{170}-\frac{b}{108}$)mol | |
| C. | cL剩余气体是O2,且c=$\frac{a}{4}$ | |
| D. | 将mgAgNO3溶于水,再加足量的盐酸,$\frac{b}{108}$×143.5g可生成沉淀 |