题目内容
11.酸碱质子理论的要点是:凡能给出质子(即H+)的分子或离子都是酸;凡能接受质子的分子或离子都是碱.按此观点,下列微粒既属于酸又属于碱的是( )①H2O ②CO32-③Al3+ ④CH3COOH ⑤NH4+ ⑥HCO3-.
| A. | ②③ | B. | ①⑥ | C. | ④⑥ | D. | ⑤⑥ |
分析 凡能给出质子(即H+)的分子或离子都是酸;凡能接受质子的分子或离子都是碱,则能给出质子且能接受质子的分子或离子既属于酸又属于碱,据此分析解答.
解答 解:凡能给出质子(即H+)的分子或离子都是酸;凡能接受质子的分子或离子都是碱,则能给出质子且能接受质子的分子或离子既属于酸又属于碱,①⑥能给出质子也能接受质子,所以既属于酸又属于碱;
②③只能接受质子,所以属于碱;④⑤只能给出质子,属于酸,故选B.
点评 本题考查酸碱判断,为高频考点,明确酸碱概念特点是解本题关键,对于概念型习题紧扣概念分析解答即可,属于基础题,难度不大.

练习册系列答案
相关题目
1.铍(Be)为第2周期第IIA族元素,根据它在元素周期表中的位置推测,铍可能具有的性质是( )
| A. | 铍原子的半径小于硼原子的半径 | |
| B. | 相同条件下,单质铍与酸反应比单质锂与酸反应剧烈 | |
| C. | 氢氧化铍的碱性比氢氧化钙的碱性弱 | |
| D. | 单质铍能与冷水剧烈反应 |
2.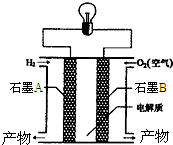 氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
 氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | B电极上发生氧化反应 | |
| B. | A电极是负极 | |
| C. | 该电池的总反应为2H2+O2=2H2O | |
| D. | 外电路中电子由A电极通过导线流向B电极 |
19.下列电子式书写不正确的是( )
| A. | 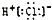 | B. | 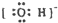 | C. | 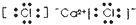 | D. | 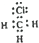 |
6.下列各组物质中化学键的类型相同的是( )
| A. | HF MgCl2 NH4Cl | B. | H2S Na2O ? CO2 | ||
| C. | CaCl2 ? NaOH C H4 | D. | NH3 H2O CS2 |
16.NA表示阿伏加德罗常数的值,则关于热化学方程式:C2H2(g)+2.5O2(g)═2CO2(g)+H2O(l)△H=-1 300kJmol-1的说法中,正确的是( )
| A. | 当5NA个电子转移时,该反应放出650 kJ的热量 | |
| B. | 当1NA个水分子生成且为气体时,放出多于1300 kJ的热量 | |
| C. | 当2 NA个碳氧双键生成时,放出1300 kJ的热量 | |
| D. | 当4NA个碳氧共用电子对生成时,放出1300kJ的热量 |
3.下列事实不能用分子间作用力解释的是( )
| A. | HF、H2O的沸点比HCl、H2S的沸点高很多 | |
| B. | 正戊烷的沸点比新戊烷的沸点高 | |
| C. | 邻羟基苯甲酸的沸点比对羟基苯甲酸的低 | |
| D. | Na2O的熔点比MgO的熔点低 |
20.砹是第七主族第六周期的元素,推测砹或砹的化合物最不可能具有的性质是( )
| A. | HAt很稳定 | B. | 砹易溶于某些有机溶剂 | ||
| C. | AgAt不溶于水 | D. | 砹是有色固体 |