题目内容
19.金属A能够被磁铁所吸引.A及其A的化合物之间有如下的转化关系: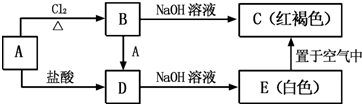
(1)写出A、C的化学式:AFe;CFe(OH)3.
(2)检验B中阳离子的试剂是KSCN溶液或NaOH溶液.
(3)写出下列反应的化学方程式或离子方程式:
A→D 的离子方程式Fe+2H+═Fe2++H2↑
E→C 的化学方程式4Fe(OH)2+2H2O+O2═4Fe(OH)3.
分析 金属A能够被磁铁所吸引,则A是Fe,Fe在氯气中燃烧生成B为FeCl3,Fe和HCl反应生成FeCl2和H2,FeCl3和Fe反应生成FeCl2,则D为FeCl2,B和NaOH反应生成红褐色的C为Fe(OH)3,D和NaOH溶液反应生成的白色E为Fe(OH)2,Fe(OH)2和氧气、水反应生成Fe(OH)3,再结合题目分析解答.
解答 解:金属A能够被磁铁所吸引,则A是Fe,Fe在氯气中燃烧生成B为FeCl3,Fe和HCl反应生成FeCl2和H2,FeCl3和Fe反应生成FeCl2,则D为FeCl2,B和NaOH反应生成红褐色的C为Fe(OH)3,D和NaOH溶液反应生成的白色E为Fe(OH)2,Fe(OH)2和氧气、水反应生成Fe(OH)3,
(1)通过以上分析知,A、C分别是Fe、Fe(OH)3,故答案为:Fe; Fe(OH)3;
(2)B为氯化铁,铁离子用KSCN或NaOH溶液检验,铁离子和KSCN混合后溶液呈血红色,和NaOH反应生成红褐色沉淀,所以可以用KSCN或NaOH溶液检验,
故答案为:KSCN溶液或NaOH溶液;
(3)Fe和稀盐酸反应生成氯化亚铁和氢气,离子方程式为Fe+2H+═Fe2++H2↑,
氢氧化亚铁和氧气、水反应生成氢氧化铁,反应方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3,
故答案为:Fe+2H+═Fe2++H2↑;4Fe(OH)2+2H2O+O2═4Fe(OH)3.
点评 本题以Fe及其化合物之间的转化为载体考查无机物推断,还涉及离子方程式书写、离子检验等知识点,明确物质性质、基本理论是解本题关键,知道铁离子、亚铁离子的检验方法及实验现象,题目难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
9.下列溶液暴露在空气中不会变质的是( )
| A. | NaCl 溶液 | B. | NaOH 溶液 | C. | 氯水 | D. | Na2SO3 溶液 |
10.‘铜和镁的合金2.14g完全溶于一定浓度的硝酸,若反应中硝酸被还NO2、NO、N2O三种气体而且在标准状况下它们的体积均为0.224L.在反应后的溶液中,加人足量的氢氧化钠溶液,生成的沉淀经过滤、洗涤、干燥后称量,质量为( )
| A. | 4.18 g | B. | 3.12 g | C. | 4.68 g | D. | 5.08 g |
7.当光束通过下列分散系,能观察到丁达尔现象的是( )
| A. | 稀硫酸 | B. | 酒精 | C. | 氢氧化铁胶体 | D. | 食盐水 |
14.Cu+2FeCl3=CuCl2+2FeCl2的反应中,做氧化剂的是( )
| A. | Cu | B. | FeCl3 | C. | CuCl2 | D. | FeCl2 |
4.对于反应: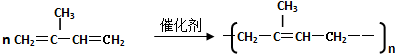 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 该反应的类型是缩聚反应 | |
| B. | 产物中链节的式量比反应物单体的分子量大 | |
| C. | 工业上用该反应生产顺丁橡胶 | |
| D. | 不同产物分子的聚合度可能不同 |
11.现将金属镁和铝的混合物9.9g完全溶解于500mL稀硝酸中,金属完全溶解(硝酸的还原产物只有NO).向所得溶液中加入烧碱溶液至金属离子恰好完全沉淀,得到沉淀25.2g,则硝酸的浓度可能为( )
| A. | 1.2mol/L | B. | 2.0mol/L | C. | 2.4mol/L | D. | 3.0mol/L |
8.下列关于物质的量浓度的叙述正确的是( )
| A. | 含1mol溶质的任何溶液,物质的量浓度一定相等 | |
| B. | 体积相同,物质的量浓度相同的同种溶液所含溶质的粒子数一定相同 | |
| C. | 1L0.5mol•L-1CaCl2溶液中,Ca2+与Cl-的物质的量浓度都是0.5mol•L-1 | |
| D. | 从1L0.2mol•LNaOH溶液中取出100ml,这100ml溶液的物质的量浓度是0.02mol•L-1 |
1.实现下列变化时,需克服相同类型作用力的是( )
| A. | 金刚石和干冰的熔化 | B. | 纯碱和烧碱的熔化 | ||
| C. | 氯化铵和水的分解 | D. | 食盐和冰醋酸熔化 |