籾朕坪否
20⤴厮岑N2+3H2?NH3@H〽0⇧孖嗤a、b、c眉倖否持屢揖議否匂⤴a否匂葎冴否拝辛參嚥翌順序佩犯住算議廾崔⇧b否匂葎冴儿拝辛參才翌順序佩犯住算議廾崔⇧c否匂葎冴否蒸犯廾崔⤴壓眉倖否匂嶄脅紗秘1molN2才3molH2⇧輝郡哘器欺峠財朔⇧眉倖否匂嶄郡哘麗廬晒楕議寄弌購狼頁↙ ⇄| A⤴ | a﹅b﹅c | B⤴ | b﹅a﹅c | C⤴ | c﹅b﹅a | D⤴ | b﹅c﹅a |
蛍裂 屢揖梁業和⇧壓悶持屢吉議畜液否匂⇧a葎冴梁冴否否匂⇧b否匂葎冴儿拝辛參才翌順序佩犯住算議廾崔⇧c葎冴否蒸犯否匂⇧軟兵麗嵎議楚屢揖⇧乎郡哘頁賑悶悶持受弌議慧犯郡哘⇧c議梁業寄噐a⇧b否匂葎冴儿拝辛參才翌順序佩犯住算議廾崔⇧b嶄儿膿寄噐a⇧功象儿膿、梁業斤峠財議唹峒登僅•
盾基 盾⦿厮岑N2+3H2?NH3@H〽0⇧郡哘頁賑悶悶持受弌議慧犯郡哘⇧屢揖梁業和⇧壓悶持屢吉議畜液否匂⇧a葎冴梁冴否否匂⇧b否匂葎冴儿拝辛參才翌順序佩犯住算議廾崔⇧c葎冴否蒸犯否匂⇧軟兵麗嵎議楚屢揖⇧乎郡哘頁賑悶悶持受弌議慧犯郡哘⇧c議梁業寄噐a⇧郡哘麗議廬晒楕受弌⇧a﹅c⇧b否匂葎冴儿拝辛參才翌順序佩犯住算議廾崔⇧b嶄儿膿寄噐a⇧郡哘麗廬晒楕b﹅a⇧郡哘麗議廬晒楕議購狼b﹅a﹅c⇧絞僉B⤴
泣得 云籾深臥阻晒僥峠財唹峒咀殆⇧否匂蒙尢、晒僥峠財卞強圻尖⇧廣吭冴梁冴否否匂、冴梁冴儿否匂、冴否蒸犯否匂個延訳周斤峠財議蛍裂圭隈⇧籾朕佃業嶄吉⤴

膳楼過狼双基宛
屢購籾朕
12⤴和双傍隈屎鳩議頁↙ ⇄
| A⤴ | 滅窃、嗟妛才軌易嵎脅頁互蛍徨晒栽麗 | |
| B⤴ | 厰桓才厰磨脅嬬嚥署奉墜郡哘伏撹狽賑 | |
| C⤴ | 牛頚↙C6H10O5⇄n才亘略殆↙C6H10O5⇄n札葎揖蛍呟更悶 | |
| D⤴ | 墳嗟議蛍蒼才炭議孤蒼譲峪窟伏麗尖延晒 |
4⤴和燕嶄糞刮荷恬嬬器欺糞刮朕議頁↙ ⇄
| 僉𡸴 | 糞刮荷恬 | 糞刮朕議 |
| A | 﨑遮磨墜卑匣嶄紗仟崙議Cu↙OH⇄2旺紗犯 | 鳩協遮磨墜醤嗤肌児來嵎 |
| B | 紗粤邦⇧尅鬼⇧狛陀茅肇柿牛 | 茅肇噂嶄詞嗤議噂罫 |
| C | 公娘磨墜卑匣嶄紗秘敵冦磨⇧繍恢伏議賑悶宥秘噂罫墜卑匣 | 刮屬磨來⦿ 冦磨﹅娘磨﹅噂罫 |
| D | 柁厰莱才狽剳晒墜議厰桓卑匣慌犯⇧繍恢伏議賑悶宥秘磨來互談磨蛇卑匣 | 刮屬恢伏議賑悶葎厰路 |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |
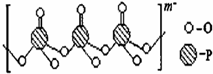 宋汽嵎式凪晒栽麗壓垢匍伏恢嶄嗤彭鴻刑議哘喘⤴易宋辛喘噐崙姥互歓業議宋磨↙
宋汽嵎式凪晒栽麗壓垢匍伏恢嶄嗤彭鴻刑議哘喘⤴易宋辛喘噐崙姥互歓業議宋磨↙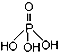 ⇄⇧眉詔宋磨墜↙NaH2PO2⇄辛喘噐晒僥尭程吉吉⤴萩指基和双諒籾⦿
⇄⇧眉詔宋磨墜↙NaH2PO2⇄辛喘噐晒僥尭程吉吉⤴萩指基和双諒籾⦿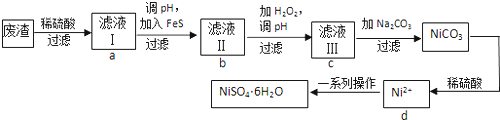

 ⤴
⤴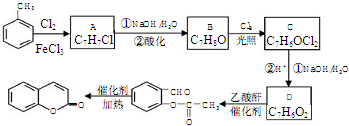
 ⇧A★B議郡哘窃侏頁函旗郡哘⤴
⇧A★B議郡哘窃侏頁函旗郡哘⤴ ⇄郡哘⇧茅伏撹
⇄郡哘⇧茅伏撹 翌⇧揖扮伏撹議総匯嶽恢麗議潤更酒塀頁CH3COOH⤴
翌⇧揖扮伏撹議総匯嶽恢麗議潤更酒塀頁CH3COOH⤴ 札葎揖蛍呟更悶⇧拝醤嗤參和蒙泣⦿
札葎揖蛍呟更悶⇧拝醤嗤參和蒙泣⦿ A、B、C、D、E、F葎念膨巓豚圻徨會方卆肝奐寄議鎗嶽圷殆⇧A、C、D圻徨譲嗤曾倖隆撹斤窮徨⇧A、B、C揖巓豚⇧A嚥D、B嚥F蛍艶揖麼怛⇧E頁伏試嶄喘楚恷寄議署奉⤴萩指基和双諒籾
A、B、C、D、E、F葎念膨巓豚圻徨會方卆肝奐寄議鎗嶽圷殆⇧A、C、D圻徨譲嗤曾倖隆撹斤窮徨⇧A、B、C揖巓豚⇧A嚥D、B嚥F蛍艶揖麼怛⇧E頁伏試嶄喘楚恷寄議署奉⤴萩指基和双諒籾 ◉亟竃A蛍徨嶄郊嬬妖議兆各忞児、忡児◉
◉亟竃A蛍徨嶄郊嬬妖議兆各忞児、忡児◉ ◉
◉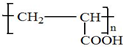 ⤴
⤴