题目内容
25℃时,将0.2mol KF固体溶于100mL 1mol?L-1 HBr溶液中,加水稀释得到1L溶液,若此溶液中c(F-)>c(Br-),下列判断不正确的是( )
| A、该溶液的pH小于7 |
| B、c(HF)+c(F-)=0.2 mol?L-1 |
| C、c(HF)<c(F-) |
| D、c(F-)+c(OH-)=0.1 mol?L-1 |
考点:离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:二者反应生成KBr和HF,HF是弱酸,溶液中的溶质是等物质的量浓度的HF、KBr、KF,若此溶液中c(F-)>c(Br-),说明HF的电离程度大于F-的水解程度,溶液呈酸性,再结合物料守恒解答.
解答:
解:二者反应生成KBr和HF,HF是弱酸,溶液中的溶质是等物质的量浓度的HF、KBr、KF,若此溶液中c(F-)>c(Br-),说明HF的电离程度大于F-的水解程度,溶液呈酸性,
A.溶液呈酸性,则pH<7,故A正确;
B.溶液中存在物料守恒,根据物料守恒得c(HF)+c(F-)=0.2 mol?L-1,故B正确;
C.若此溶液中c(F-)>c(Br-),说明HF的电离程度大于F-的水解程度,所以溶液呈存在c(HF)<c(F-),故C正确;
D.根据电荷守恒得c(H+)+c(K+)=c(OH-)+c(F-)+c(Br-),根据物料守恒得c(K+)=2c(Br-),则c(H+)+c(Br-)=c(OH-)+c(F-),c(Br-)=0.1mol/L,所以c(H+)+c(Br-)=c(OH-)+c(F-)>0.1mol/L,故D错误;
故选D.
A.溶液呈酸性,则pH<7,故A正确;
B.溶液中存在物料守恒,根据物料守恒得c(HF)+c(F-)=0.2 mol?L-1,故B正确;
C.若此溶液中c(F-)>c(Br-),说明HF的电离程度大于F-的水解程度,所以溶液呈存在c(HF)<c(F-),故C正确;
D.根据电荷守恒得c(H+)+c(K+)=c(OH-)+c(F-)+c(Br-),根据物料守恒得c(K+)=2c(Br-),则c(H+)+c(Br-)=c(OH-)+c(F-),c(Br-)=0.1mol/L,所以c(H+)+c(Br-)=c(OH-)+c(F-)>0.1mol/L,故D错误;
故选D.
点评:本题考查了离子浓度大小比较,根据溶液中的溶质及HF的电离程度和F-的水解程度相对大小确定溶液酸碱性,再结合电荷守恒、物料守恒来分析解答,题目难度中等.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
部分弱酸在水溶液中的电离平衡常数如下表
下列选项正确的是( )
| 弱酸 | 氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
| 电离平衡常数K (25℃) |
K=4.93×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
K=3.53×10-4 |
| A、NaCN溶液中通入少量CO2:CN-+H2O+CO2→HCN+HCO3- |
| B、Na2CO3溶液中通入少量HF:CO32-+2HF→2F-+CO2+H2O |
| C、25℃,等浓度的NaCN和NaF溶液中pH值前者大于后者 |
| D、中和等体积、等pH的HCN和HF消耗NaOH的量前者小于后者 |
下列反应的化学方程式正确的是( )
A、合成聚乙烯塑料: | |||
B、溴乙烷与氢氧化钠溶液共热:CH3CH2Br+NaOH
| |||
C、向稀苯酚溶液中滴加少量浓溴水:2 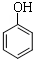 +3Br2→2 +3Br2→2 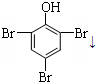 ↓ ↓ | |||
D、实验室制乙烯:CH3CH2OH
|
钠和水反应时所产生的现象可以体现钠的下列性质中的( )
| A、钠的沸点低 |
| B、钠的硬度大 |
| C、钠的密度小 |
| D、钠有强的还原性 |
室温下,对于0.10mol?L-1的氨水,下列判断正确的是( )
| A、用相同浓度的HNO3溶液中和,硝酸体积小于氨水时,溶液可能呈中性 |
| B、温度不变,加水稀释后溶液中c(NH4+)?c(OH-)不变 |
| C、加水稀释后,溶液中导电粒子的数目减少 |
| D、其溶液的pH=13 |
下列有关四个电化学装置的叙述正确的是( )


| A、图Ⅰ装置中MnO2作催化剂 |
| B、图Ⅱ装置工作一段时间后,滴加少量K3[Fe(CN)6]溶液,无明显现象 |
| C、图Ⅲ装置中Cu作阳极,为电解液提供Cu2+,保持溶液中Cu2+浓度恒定 |
| D、图Ⅳ装置工作时,为平衡电荷,a烧杯中的Zn2+经盐桥移向b烧杯中 |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,工作原理如图如示.下列有关说法正确的是( )

| A、当有0.2 mol电子转移时,a电极产生2.24 L H2 |
| B、b电极上发生的电极反应式为2H++2e-═H2↑ |
| C、d电极上发生的电极反应式为O2+4H++4e-═2H2O |
| D、d电极上进行氧化反应,B池中的H+可以通过隔膜进入A池 |
