题目内容
碳酸钾与碳酸氢钾都是重要的化学试剂与工业原料,具有广泛的用途.
(1)将碳酸钾、石灰石和二氧化硅进行高温煅烧,可得到组成为K2O?CaO?6SiO2的钾玻璃,同时排出CO2.若制造5.1kg钾玻璃,排放的CO2在标准状况下的体积是 L.
(2)已知亚硫酸的酸性强于碳酸.工业上用碳酸钾与碳酸氢钾的混合溶液吸收SO2,充分反应后,所得溶液组成如下表:
计算原吸收液中碳酸钾与碳酸氢钾的物质的量之比.
(3)根据上表中的数据,计算上表的混合溶液还能吸收SO2的最大质量(不计SO2的溶解).
(4)将热的浓CuSO4溶液与K2CO3溶液混合,析出物中有一种蓝色粒状晶体(不含结晶水),式量为376,其中钾元素的质量分数为0.104.取0.02mol该晶体溶于足量的稀盐酸中,没有气体产生,再加入BaCl2,产生9.32g白色沉淀,通过计算推断晶体的化学式.
(1)将碳酸钾、石灰石和二氧化硅进行高温煅烧,可得到组成为K2O?CaO?6SiO2的钾玻璃,同时排出CO2.若制造5.1kg钾玻璃,排放的CO2在标准状况下的体积是
(2)已知亚硫酸的酸性强于碳酸.工业上用碳酸钾与碳酸氢钾的混合溶液吸收SO2,充分反应后,所得溶液组成如下表:
| 物质 | K2CO3 | KHCO3 | K2SO3 |
| 质量(kg) | 55.2 | 120.0 | 63.2 |
(3)根据上表中的数据,计算上表的混合溶液还能吸收SO2的最大质量(不计SO2的溶解).
(4)将热的浓CuSO4溶液与K2CO3溶液混合,析出物中有一种蓝色粒状晶体(不含结晶水),式量为376,其中钾元素的质量分数为0.104.取0.02mol该晶体溶于足量的稀盐酸中,没有气体产生,再加入BaCl2,产生9.32g白色沉淀,通过计算推断晶体的化学式.
考点:化学方程式的有关计算,有关混合物反应的计算,复杂化学式的确定
专题:计算题
分析:(1)组成为K2O?CaO?6SiO2的钾玻璃,n=
=10mol,由K2O?CaO~K2CO3?CaCO3~2CO2↑计算;
(2)n(K2CO3)=0.4mol,n(KHCO3)=1.2mol,n(K2SO3)=0.4mol,结合2K2CO3+SO2+H2O→2KHCO3+K2SO3反应计算;
(3)混合溶液还能吸收SO2的最大质量时生成KHSO3,结合原子守恒计算;
(4)n(K+)=
=0.02mol,产生9.32g白色沉淀为硫酸钡,n(SO42-)=
=0.04mol,没有气体,不含碳酸根离子,蓝色粒状晶体含铜离子,结合相对分子质量分析.
| 5100g |
| 510g/mol |
(2)n(K2CO3)=0.4mol,n(KHCO3)=1.2mol,n(K2SO3)=0.4mol,结合2K2CO3+SO2+H2O→2KHCO3+K2SO3反应计算;
(3)混合溶液还能吸收SO2的最大质量时生成KHSO3,结合原子守恒计算;
(4)n(K+)=
| 376×0.02×0.104 |
| 39 |
| 9.32g |
| 233g/mol |
解答:
解:(1)组成为K2O?CaO?6SiO2的钾玻璃,n=
=10mol,由K2O?CaO~K2CO3?CaCO3~2CO2↑可知,生成气体为20mol,体积为20mol×22.4L/mol=448L,
故答案为:448;
(2)n(K2CO3)=0.4kmol,n(KHCO3)=1.2kmol,n(K2SO3)=0.4kmol,由2K2CO3+SO2+H2O→2KHCO3+K2SO3,K2CO3原有0.4+0.8=1.2kmol,KHCO3原有1.2-0.8=0.4kmol,原吸收液中碳酸钾与碳酸氢钾的物质的量之比为3:1,
故答案为:碳酸钾与碳酸氢钾的物质的量之比为3:1;
(3)混合溶液还能吸收SO2的最大质量时生成KHSO3,K+总和为2.8kmol,最多可形成KHSO32.8kmol,故还可吸收SO2为2.8-0.4=2.4kmol,其质量为2.4kmol×64g/mol=153.6kg,答:能吸收SO2的最大质量为153.6kg;
(4)n(K+)=
=0.02mol,产生9.32g白色沉淀为硫酸钡,n(SO42-)=
=0.04mol,没有气体,不含碳酸根离子,蓝色粒状晶体含铜离子,钾离子与硫酸根离子个数比为1:2,若铜离子个数为2,由电荷守恒可知,OH-的个数为1,化学式为KCu2(OH)(SO4)2,其式量为376符合题意,
答:晶体的化学式为KCu2(OH)(SO4)2.
| 5100g |
| 510g/mol |
故答案为:448;
(2)n(K2CO3)=0.4kmol,n(KHCO3)=1.2kmol,n(K2SO3)=0.4kmol,由2K2CO3+SO2+H2O→2KHCO3+K2SO3,K2CO3原有0.4+0.8=1.2kmol,KHCO3原有1.2-0.8=0.4kmol,原吸收液中碳酸钾与碳酸氢钾的物质的量之比为3:1,
故答案为:碳酸钾与碳酸氢钾的物质的量之比为3:1;
(3)混合溶液还能吸收SO2的最大质量时生成KHSO3,K+总和为2.8kmol,最多可形成KHSO32.8kmol,故还可吸收SO2为2.8-0.4=2.4kmol,其质量为2.4kmol×64g/mol=153.6kg,答:能吸收SO2的最大质量为153.6kg;
(4)n(K+)=
| 376×0.02×0.104 |
| 39 |
| 9.32g |
| 233g/mol |
答:晶体的化学式为KCu2(OH)(SO4)2.
点评:本题考查化学反应方程式的计算,题目难度较大,把握发生的化学反应及原子守恒为解答的关键,侧重分析能力及计算能力的考查,(4)为解答的难点.

练习册系列答案
相关题目
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).能判断该反应是否达到化学平衡状态的依据是( )
| A、容器中压强不变 |
| B、单位时间内消耗了n mol CO2,同时生成了n mol H2O |
| C、v正(H2)=v逆(H2O) |
| D、c(CO2)=c(CO) |
戊烷(C5H12)的同分异构体共有( )个.
| A、2个 | B、3个 | C、4个 | D、5个 |
25℃时,将0.2mol KF固体溶于100mL 1mol?L-1 HBr溶液中,加水稀释得到1L溶液,若此溶液中c(F-)>c(Br-),下列判断不正确的是( )
| A、该溶液的pH小于7 |
| B、c(HF)+c(F-)=0.2 mol?L-1 |
| C、c(HF)<c(F-) |
| D、c(F-)+c(OH-)=0.1 mol?L-1 |

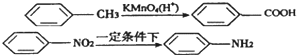
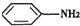 (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)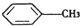 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物.
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物.