题目内容
6.现有10种元素的性质、数据如下表所列,它们均为短周期元素.| A | B | C | D | E | F | G | H | I | J | |
| 原子半径 (10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | 1.02 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6 | +1 | |
| -2 | -3 | -1 | -3 | -2 |
(1)D在元素周期表中的位置第三周期第VA族,若H的一种同位素中子数为5,则其原子符号是510B,B元素的原子结构示意图是
 ,G与F分别形成的简单离子半径大小关系为N3->Na+.
,G与F分别形成的简单离子半径大小关系为N3->Na+.(2)F与A形成的化合物电子式是:
 、
、 .
.(3)用电子式表示F2I的形成过程:
 ;
;(4)F与J形成的化合物电子式为
 ,该化合物与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑..
,该化合物与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑..
分析 由表格在元素的性质可知,+1价的C、F、J,结合原子半径可知,F为Na,C为Li,J为H;A、I均有-2价,且A只有-2价,则A为O,I为S;B最高化合价为+2价,应为第二主族元素,且原子半径F>B>C,则B为Mg元素,D和G最高正价均为+5,负价一致,故为VA族元素,因原子半径D>G,故D为第三周期第VA族的P元素,G为N元素;从化合价可推出E属于卤素,由于短周期F元素无正价,故E为氯元素,位于第VIIA族第三周期;H最高正价+3价,无负价,只能是IIIA族元素,而原子半径H>F,故H只能是位于第二周期第IIIA族的B元素,以此解答该题.
解答 解:由表格在元素的性质可知,+1价的C、F、J,结合原子半径可知,F为Na,C为Li,J为H;A、I均有-2价,且A只有-2价,则A为O,I为S;B最高化合价为+2价,应为第二主族元素,且原子半径F>B>C,则B为Mg元素,D和G最高正价均为+5,负价一致,故为VA族元素,因原子半径D>G,故D为第三周期第VA族的P元素,G为N元素;从化合价可推出E属于卤素,由于短周期F元素无正价,故E为氯元素,位于第VIIA族第三周期;H最高正价+3价,无负价,只能是IIIA族元素,而原子半径H>F,故H只能是位于第二周期第IIIA族的B元素,
(1)由以上分析可知,D为磷元素,原子序数为15,位于周期表中第三周期第VA族;
H为B元素,若H的一种同位素中子数为5,则其原子符号是510B;
Mg元素的原子序数为12,其原子结构示意图是 ;
;
N3->Na+的电子层数相同,核电荷数越大离子半径越小,则离子半径大小为:N3->Na+,
故答案为:第三周期第VA族;510B;  ;N3->Na+;
;N3->Na+;
(2)Na、O形成的化合物为氧化钠、过氧化钠,二者都是离子化合物,其电子式为 、
、 ,
,
故答案为: 、
、 ;
;
(3)F2I为Na2S,Na2S为离子化合物,用电子式表示Na2S的形成过程为 ,
,
故答案为: ;
;
(4)F、J分别为Na、H元素,二者形成的化合物为NaH,NaH为离子化合物,其电子式为 ;NaH与水反应生成氢氧化钠和氢气,反应的化学方程式为:NaH+H2O=NaOH+H2↑,
;NaH与水反应生成氢氧化钠和氢气,反应的化学方程式为:NaH+H2O=NaOH+H2↑,
故答案为: ;NaH+H2O=NaOH+H2↑.
;NaH+H2O=NaOH+H2↑.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的化合价、原子半径推断元素为解答的关键,侧重分析与应用能力的考查,注意电子式表示形成过程、原电池原理的应用等为解答的难点,题目难度不大.

(一)测定目的:测定×××牌软包装橙汁中维生素C的含量.
(二)测定原理:C6H8O6+I2→C6H6O6+2H++2I-
(三)实验用品及试剂
(1)仪器和用品(自选,略)
(2)试剂:指示剂淀粉溶液(填名称),浓度为8.00×10-3mol•L-1的I2标准溶液、蒸馏水等.
(四)实验过程
(3)洗涤仪器,检查滴定管是否漏液,润洗相关仪器后,装好标准碘溶液待用.
(4)用酸式滴定管(填仪器名称)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂.
(5)用左手控制滴定管的活塞(填部位),右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直到滴定终点.滴定至终点时的现象是最后一滴标准液滴入时,溶液由无色变为蓝色,且半分钟内不褪色.
(五)数据记录与处理
| 起始(mL) | 终点(mL) | |
| 1 | 5.00 | 20.02 |
| 2 | 3.00 | 18.00 |
| 3 | 4.00 | 18.98 |
(六)问题讨论
(7)从分析数据看,此软包装橙汁是否是纯天然橙汁?不是(填“是”或“不是”或“可能是”,1分).生产商最可能采取的做法是B(填编号):
A.加水稀释天然橙汁 B.将维生素C作为添加剂 C.橙汁已被浓缩.
(1)表列举了不同温度下大气固氮和工业固氮的部分K值.
| 反应 | 大气固氮 N2 (g)+O2 (g)?2NO(g) | 工业固氮 N2 (g)+3H2 (g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,但从催化剂活性等综合因素考虑选择500℃左右合适.
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较р1、р2的大小关系р1<р1.(填“<”、“>”或者“=”)


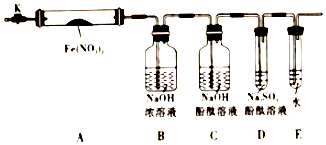 固体硝酸盐加热易分解且产物较复杂,某学习小组以Fe(NO3)2为研究对象,通过实验探究其热分解的产物,查阅资料,根据硝酸盐受热分解的规律,提出如下4种猜想:
固体硝酸盐加热易分解且产物较复杂,某学习小组以Fe(NO3)2为研究对象,通过实验探究其热分解的产物,查阅资料,根据硝酸盐受热分解的规律,提出如下4种猜想: W、X、Y、Z 是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知 Y、Z 两种元素的单质是空气的主要成分,W 原子的最外层电子数与 Ne 原子的最外层电子数相差 1.
W、X、Y、Z 是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知 Y、Z 两种元素的单质是空气的主要成分,W 原子的最外层电子数与 Ne 原子的最外层电子数相差 1. 将1mol I2(g) 和2mol H2置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)△H<0,并达平衡.HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
将1mol I2(g) 和2mol H2置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)△H<0,并达平衡.HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示: