��Ŀ����
����FeCl3��AlCl3�Ļ����Һ100mL����μ���NaOH��Һ�����ɳ��������ʵ���������NaOH�����ʵ����Ĺ�ϵ��ͼ��

��1��a���Ӧ�ij���Ϊ ���ѧʽ����
��2������ԭ���Һ��FeCl3�����ʵ���Ũ��Ϊ���٣���д��������̣�
��3����ȡԭ�����Һ50mL��������0.5mol��������µĻ����Һ�����µĻ����Һ����μ���NaOH��Һ�����������ڻ������ɳ��������ʵ���������NaOH�����ʵ����Ĺ�ϵͼ��

��1��a���Ӧ�ij���Ϊ
��2������ԭ���Һ��FeCl3�����ʵ���Ũ��Ϊ���٣���д��������̣�
��3����ȡԭ�����Һ50mL��������0.5mol��������µĻ����Һ�����µĻ����Һ����μ���NaOH��Һ�����������ڻ������ɳ��������ʵ���������NaOH�����ʵ����Ĺ�ϵͼ��
���㣺þ��������Ҫ������,��ѧ����ʽ���йؼ���
ר�⣺ͼʾ��
�����������ǿ������κ������������Ӧ����Ͻ�ϻ�ѧ�仯��ͼ��Ĺ�ϵ���������
AlCl3+3NaOH�TAl��OH��3��+3NaCl��Al��OH��3+NaOH�TNaAlO2+2H2O��
FeCl3+3NaOH�TFe��OH��3��+3NaCl�仯����ѧ����Ϊ���ȳ��ֳ�����������ܽ�һ���֣��������������䣬���й����ݽ�Ϸ�Ӧ��ϵ��������ݻ�ѧ�仯���̼����Ĺ�ϵ����ͼ��
AlCl3+3NaOH�TAl��OH��3��+3NaCl��Al��OH��3+NaOH�TNaAlO2+2H2O��
FeCl3+3NaOH�TFe��OH��3��+3NaCl�仯����ѧ����Ϊ���ȳ��ֳ�����������ܽ�һ���֣��������������䣬���й����ݽ�Ϸ�Ӧ��ϵ��������ݻ�ѧ�仯���̼����Ĺ�ϵ����ͼ��
���
�⣺��FeCl3��AlCl3�Ļ����Һ����μ���NaOH��Һ�ֱ������·�Ӧ��
AlCl3+3NaOH�TAl��OH��3��+3NaCl��FeCl3+3NaOH�TFe��OH��3��+3NaCl��
Al��OH��3+NaOH�TNaAlO2+2H2O���ݷ�Ӧ����ʽ�Ĺ�ϵ�ó������������������������������ֳ�����������ͼ����Ϊa��ʱ�������������������Һ�е�FeCl3��AlCl3�պ���ȫ��Ӧ����a�����ΪFe��OH��3��Al��OH��3��
�ʴ�Ϊ��Fe��OH��3��Al��OH��3��
��2������ͼ��Ĺ�ϵ����Ϸ�Ӧ����ʽAlCl3+3NaOH�TAl��OH��3��+3NaCl��FeCl3+3NaOH�TFe��OH��3��+3NaCl������Һ����3mol��������ʱ������Һ�е�FeCl3��AlCl3��NaOH�պ���ȫ��Ӧ������Al��OH��3��Fe��OH��3�������ټ���������3.6molʱ�������������ֲ��䣬�ַ���
Al��OH��3+NaOH�TNaAlO2+2H2O������b��ʱ����ȫ��ΪFe��OH��3�����У�
��a��ʱAl��OH��3�����ʵ���Ϊx mol��
Al��OH��3+NaOH�TNaAlO2+2H2O
1 1
x mol ��3.6-3��mol
����1��1=x mol����3.6-3��mol
��ã�x=0.6��mol����
����ԭ�����Һ��AlCl3��Ӧ��NaOH�����ʵ���Ϊy mol��
AlCl3+3NaOH�TAl��OH��3��+3NaCl
3 1
y mol 0.6mol
����3��1=y mol��0.6 mol
��ã�y=1.8��mol����
��ԭ�����Һ��FeCl3�����ʵ���Ϊz mol��
FeCl3+3NaOH�TFe��OH��3��+3NaCl
1 3
z mol ��3-1.8��mol
����1��3=z mol����3-1.8��mol��
��ã�z=0.4��mol����
��ԭ���Һ��FeCl3�����ʵ���Ũ��Ϊ0.4mol/0.1L=4mol/L��
�ʴ�Ϊ��4mol/L��
��3������ȡԭ��Һ50mL������0.5mol����õ�����Һ�����еijɷ��У�FeCl3��AlCl3��HCl�������м���NaOH��Һʱ���ȷ���HCl+NaOH�TNaCl+H2O��Ӧ������HCl��Ӧ����ڷ�����FeCl3��AlCl3�����ɳ���������ʽΪ��AlCl3+3NaOH�TAl��OH��3��+3NaCl��FeCl3+3NaOH�TFe��OH��3��+3NaCl��
��ȫ��Ӧ���ַ�����Ӧ Al��OH��3+NaOH�TNaAlO2+2H2O��
��50mLԭ��Һ��FeCl3��AlCl3�����ʵ����ֱ�Ϊ��0.2mol��0.3mol��
���к�0.5molHCl���ĵ�NaOH���ʵ���Ϊxmol�����У�
HCl+NaOH�TNaCl+H2O
1 1
0.5mol x
����1��1�T0.5mol��x
��ã�x�T0.5mol��
�跴Ӧ��0.4molFeCl3�������ĵ�NaOH���ʵ���Ϊymol�����У�
FeCl3+3NaOH�TFe��OH��3��+3NaCl
1 3
0.2mol y
����1��3=0.2mol��y
��ã�y�T0.6mol
�跴Ӧ��0.6molAlCl3���ĵ�NaOH���ʵ���Ϊzmol������Al��OH��3��+zmol���У�
AlCl3+3NaOH�TAl��OH��3��+3NaCl
1 3 1
0.3mol y z
����3��1=0.3 mol��y
��ã�y=1.1mol��z�T0.3mol
���ԣ���������������Һ��ԭ��Һ�е�FeCl3��AlCl3��HCl��ȫ����Ӧ���ʱ��������2mol��
�ټ���NaOH�������ɵ�Al��OH��3��Ӧ��
�跴Ӧ��0.3molAl��OH��3���ĵ�NaOH���ʵ���Ϊnmol�����У�
Al��OH��3+NaOH�TNaAlO2+2H2O
1 1
0.3mol n
����1��1�T0.3 mol��n
��ã�n=0.3mol��
��Ϸ�Ӧ����Ӧ�����Ĺ�ϵ���������ɳ��������ʵ���������NaOH�����ʵ����Ĺ�ϵͼ��
�ʴ�Ϊ��

AlCl3+3NaOH�TAl��OH��3��+3NaCl��FeCl3+3NaOH�TFe��OH��3��+3NaCl��
Al��OH��3+NaOH�TNaAlO2+2H2O���ݷ�Ӧ����ʽ�Ĺ�ϵ�ó������������������������������ֳ�����������ͼ����Ϊa��ʱ�������������������Һ�е�FeCl3��AlCl3�պ���ȫ��Ӧ����a�����ΪFe��OH��3��Al��OH��3��
�ʴ�Ϊ��Fe��OH��3��Al��OH��3��
��2������ͼ��Ĺ�ϵ����Ϸ�Ӧ����ʽAlCl3+3NaOH�TAl��OH��3��+3NaCl��FeCl3+3NaOH�TFe��OH��3��+3NaCl������Һ����3mol��������ʱ������Һ�е�FeCl3��AlCl3��NaOH�պ���ȫ��Ӧ������Al��OH��3��Fe��OH��3�������ټ���������3.6molʱ�������������ֲ��䣬�ַ���
Al��OH��3+NaOH�TNaAlO2+2H2O������b��ʱ����ȫ��ΪFe��OH��3�����У�
��a��ʱAl��OH��3�����ʵ���Ϊx mol��
Al��OH��3+NaOH�TNaAlO2+2H2O
1 1
x mol ��3.6-3��mol
����1��1=x mol����3.6-3��mol
��ã�x=0.6��mol����
����ԭ�����Һ��AlCl3��Ӧ��NaOH�����ʵ���Ϊy mol��
AlCl3+3NaOH�TAl��OH��3��+3NaCl
3 1
y mol 0.6mol
����3��1=y mol��0.6 mol
��ã�y=1.8��mol����
��ԭ�����Һ��FeCl3�����ʵ���Ϊz mol��
FeCl3+3NaOH�TFe��OH��3��+3NaCl
1 3
z mol ��3-1.8��mol
����1��3=z mol����3-1.8��mol��
��ã�z=0.4��mol����
��ԭ���Һ��FeCl3�����ʵ���Ũ��Ϊ0.4mol/0.1L=4mol/L��
�ʴ�Ϊ��4mol/L��
��3������ȡԭ��Һ50mL������0.5mol����õ�����Һ�����еijɷ��У�FeCl3��AlCl3��HCl�������м���NaOH��Һʱ���ȷ���HCl+NaOH�TNaCl+H2O��Ӧ������HCl��Ӧ����ڷ�����FeCl3��AlCl3�����ɳ���������ʽΪ��AlCl3+3NaOH�TAl��OH��3��+3NaCl��FeCl3+3NaOH�TFe��OH��3��+3NaCl��
��ȫ��Ӧ���ַ�����Ӧ Al��OH��3+NaOH�TNaAlO2+2H2O��
��50mLԭ��Һ��FeCl3��AlCl3�����ʵ����ֱ�Ϊ��0.2mol��0.3mol��
���к�0.5molHCl���ĵ�NaOH���ʵ���Ϊxmol�����У�
HCl+NaOH�TNaCl+H2O
1 1
0.5mol x
����1��1�T0.5mol��x
��ã�x�T0.5mol��
�跴Ӧ��0.4molFeCl3�������ĵ�NaOH���ʵ���Ϊymol�����У�
FeCl3+3NaOH�TFe��OH��3��+3NaCl
1 3
0.2mol y
����1��3=0.2mol��y
��ã�y�T0.6mol
�跴Ӧ��0.6molAlCl3���ĵ�NaOH���ʵ���Ϊzmol������Al��OH��3��+zmol���У�
AlCl3+3NaOH�TAl��OH��3��+3NaCl
1 3 1
0.3mol y z
����3��1=0.3 mol��y
��ã�y=1.1mol��z�T0.3mol
���ԣ���������������Һ��ԭ��Һ�е�FeCl3��AlCl3��HCl��ȫ����Ӧ���ʱ��������2mol��
�ټ���NaOH�������ɵ�Al��OH��3��Ӧ��
�跴Ӧ��0.3molAl��OH��3���ĵ�NaOH���ʵ���Ϊnmol�����У�
Al��OH��3+NaOH�TNaAlO2+2H2O
1 1
0.3mol n
����1��1�T0.3 mol��n
��ã�n=0.3mol��
��Ϸ�Ӧ����Ӧ�����Ĺ�ϵ���������ɳ��������ʵ���������NaOH�����ʵ����Ĺ�ϵͼ��
�ʴ�Ϊ��

������������һ����������ǿ�Ӧ������Ŀ��飬��Ҫ����ѧ�仯�����뻯ѧ����ķ�����������������仯����������ͼ���У������ۺ���ǿ����Ҫϸ�����森

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
�������ӷ���ʽ��д��ȷ���ǣ�������
| A������ͭ��Һ�м������Ba��OH��2��Һ��Ba2++SO42-=BaSO4�� |
| B��A1Cl3��Һ�мӹ�����NaOH��Һ��Al3++3OH-=Al��OH��3�� |
| C��ͭ����������Һ��Ӧ��Cu+Ag+=Cu2++Ag |
| D��̼�����������ᷴӦ��CaCO3+2H+=Ca2++CO2��+H2O |
��NA��ʾ����ӵ�������������˵������ȷ���ǣ�������
| A���ڱ�״���£�22.4L NH3���е�ԭ����ΪNA |
| B��5.6g��������������ȫ��Ӧ��ʧȥ�ĵ�����Ϊ0.2NA |
| C��1L 0.1mol/L AlCl3��Һ�У���Al3+�����ʵ���Ϊ0.1NA |
| D�����Ϊ44.8L �ĵ��������ķ��Ӹ���2NA�� |


 ��������������˵����ȷ����
��������������˵����ȷ����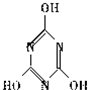 ������������ɿ���������������ͨ���ӳɷ�Ӧ�õ��Ļ�״���ӣ�������Ľṹʽ��
������������ɿ���������������ͨ���ӳɷ�Ӧ�õ��Ļ�״���ӣ�������Ľṹʽ�� A��F����ѧ�������ʣ�����B��D��F��Ϊ���ʣ����ǵ��ת����ϵ��ͼ��ʾ��
A��F����ѧ�������ʣ�����B��D��F��Ϊ���ʣ����ǵ��ת����ϵ��ͼ��ʾ��