题目内容
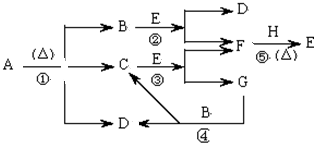
已知化合物A、D、E、G焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多.A~H各物质的变化关系如下图所示.
(1)写出A、D、E、F的化学式
A ;D ;E ;G .
(2)写出B与E反应的化学方程式:
(3)写出G溶液与B反应的离子方程式: .

(1)写出A、D、E、F的化学式
A
(2)写出B与E反应的化学方程式:
(3)写出G溶液与B反应的离子方程式:
考点:无机物的推断,钠的重要化合物
专题:推断题,几种重要的金属及其化合物
分析:化合物A、D、E、G焰色反应时,火焰均呈黄色,证明含有钠元素;其中A可用作家庭食品添加剂,也可用以治疗胃酸过多证明为NaHCO3;A分解生成二氧化碳、水、碳酸钠,D焰色反应为黄色证明为Na2CO3,E含钠元素,和水和二氧化碳反应生成F,推断E为Na2O2,依据转化关系得到B为CO2,C为H2O,F为O2,G为NaOH,H为Na,结合物质的性质以及题目要求解答该题.
解答:
解:化合物A、D、E、G焰色反应时,火焰均呈黄色,证明含有钠元素;其中A可用作家庭食品添加剂,也可用以治疗胃酸过多证明为NaHCO3;A分解生成二氧化碳、水、碳酸钠,D焰色反应为黄色证明为Na2CO3,E含钠元素,和水和二氧化碳反应生成F,推断E为Na2O2,依据转化关系得到B为CO2,C为H2O,F为O2,G为NaOH,H为Na,
(1)由以上分析可知A、D、E、G分别为NaHCO3、Na2CO3、Na2O2、NaOH,故答案为:NaHCO3;Na2CO3;Na2O2;NaOH;
(2)B为CO2,E为Na2O2,二者反应生成碳酸钠和氧气,反应的方程式为2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(3)G为NaOH,B为CO2,二者反应的离子方程式为2OH-+CO2═CO32-+H2O,故答案为:2OH-+CO2═CO32-+H2O.
(1)由以上分析可知A、D、E、G分别为NaHCO3、Na2CO3、Na2O2、NaOH,故答案为:NaHCO3;Na2CO3;Na2O2;NaOH;
(2)B为CO2,E为Na2O2,二者反应生成碳酸钠和氧气,反应的方程式为2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(3)G为NaOH,B为CO2,二者反应的离子方程式为2OH-+CO2═CO32-+H2O,故答案为:2OH-+CO2═CO32-+H2O.
点评:本题考查无机物的推断,侧重于钠及其化合物之间的转化,根据焰色反应及A的性质、用途来确定A物质,再结合物质之间的相互反应来推断其它物质,同时考查学生发散思维能力、归纳总结能力,难度中等.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
2NO(g)+O2(g)2NO2(g)△H=-112kJ/mol.在一密闭容器中充入1.0mol NO和足量氧气,充分反应后放出的热量为( )
| A、112kJ |
| B、56kJ |
| C、小于56kJ |
| D、-56kJ |
关于工业制金刚砂的反应:SiO2+3C
SiC+2CO↑,下列说法中正确的是( )
| ||
| A、SiO2是氧化剂,C为还原剂 |
| B、碳的还原性比硅强 |
| C、氧化剂和还原剂的物质的量之比为2:1 |
| D、1mol SiO2参与反应时,转移电子4mol |
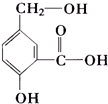 烃及烃的含氧衍生物在有机化学中占有举足轻重的地位.请根据相关知识和信息回答下列有关问题:
烃及烃的含氧衍生物在有机化学中占有举足轻重的地位.请根据相关知识和信息回答下列有关问题: