题目内容
现有部分短周期元素的性质或原子结构如下表:
(1)元素T的原子最外层共有 种不同运动状态的电子.元素X的一种同位素可测定文物年代,这种同位素的符号是
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式 (用元素符号表示)
(3)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
A、常温下Z的单质和T的单质状态不同
B、Z的氢化物比T的氢化物稳定
C、一定条件下Z和T的单质都能与氢氧化钠溶液反应
D、Z的最高价氧化物对应水化物比T的最高价氧化物对应水化物酸性强
(4)Y的气态氢化物与X的最高价氧化物对应水化物反应生成的物质属于 晶体.
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式
(3)元素Z与元素T相比,非金属性较强的是
A、常温下Z的单质和T的单质状态不同
B、Z的氢化物比T的氢化物稳定
C、一定条件下Z和T的单质都能与氢氧化钠溶液反应
D、Z的最高价氧化物对应水化物比T的最高价氧化物对应水化物酸性强
(4)Y的气态氢化物与X的最高价氧化物对应水化物反应生成的物质属于
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:T元素M层上有2对成对电子,M层上有6个电子,为S元素;
X最外层电子数是次外层电子数的2倍,最外层电子数不超过8个,则X是C元素;
Y常温下单质为双原子分子,其氢化物水溶液呈碱性,则Y是N元素;
Z元素最高正价是+7价,且为短周期元素,所以Z是Cl元素,再结合物质结构性质解答.
X最外层电子数是次外层电子数的2倍,最外层电子数不超过8个,则X是C元素;
Y常温下单质为双原子分子,其氢化物水溶液呈碱性,则Y是N元素;
Z元素最高正价是+7价,且为短周期元素,所以Z是Cl元素,再结合物质结构性质解答.
解答:
解:T元素M层上有2对成对电子,M层上有6个电子,为S元素;
X最外层电子数是次外层电子数的2倍,最外层电子数不超过8个,则X是C元素;
Y常温下单质为双原子分子,其氢化物水溶液呈碱性,则Y是N元素;
Z元素最高正价是+7价,且为短周期元素,所以Z是Cl元素,
(1)原子核外有几个电子就有几种运动状态,所以T原子核外最外层有6种运动状态,元素X的一种同位素可测定文物年代,这种碳原子有8个中子,这种同位素的符号是
C,
故答案为:6;
C;
(2)铵根离子中每个氢原子和氮原子之间共用一对电子,所以其电子式为 ,故答案为:
,故答案为: ;
;
(3)S、Cl非金属性较强的是Cl元素,
A.常温下Z的单质和T的单质状态不同与其非金属性强弱无关,故错误;
B.元素的金属性越强,其气态氢化物越稳定,Z的氢化物比T的氢化物稳定,则Z的非金属性大于T,故正确;
C.元素非金属性强弱与是否与氢氧化钠溶液反应无关,故错误;
D.元素的非金属性越强,其最高价氧化物的化合物酸性越强,Z的最高价氧化物对应水化物比T的最高价氧化物对应水化物酸性强,所以Z的非金属性大于T,故正确;
故选BD;
故答案为:Cl;BD;
(4)Y的气态氢化物为氨气,X的最高价氧化物对应水化物是碳酸,二者反应生成碳酸铵或碳酸氢铵,碳酸铵或碳酸氢铵都属于离子晶体,故答案为:离子.
X最外层电子数是次外层电子数的2倍,最外层电子数不超过8个,则X是C元素;
Y常温下单质为双原子分子,其氢化物水溶液呈碱性,则Y是N元素;
Z元素最高正价是+7价,且为短周期元素,所以Z是Cl元素,
(1)原子核外有几个电子就有几种运动状态,所以T原子核外最外层有6种运动状态,元素X的一种同位素可测定文物年代,这种碳原子有8个中子,这种同位素的符号是
14 6 |
故答案为:6;
14 6 |
(2)铵根离子中每个氢原子和氮原子之间共用一对电子,所以其电子式为
 ,故答案为:
,故答案为: ;
;(3)S、Cl非金属性较强的是Cl元素,
A.常温下Z的单质和T的单质状态不同与其非金属性强弱无关,故错误;
B.元素的金属性越强,其气态氢化物越稳定,Z的氢化物比T的氢化物稳定,则Z的非金属性大于T,故正确;
C.元素非金属性强弱与是否与氢氧化钠溶液反应无关,故错误;
D.元素的非金属性越强,其最高价氧化物的化合物酸性越强,Z的最高价氧化物对应水化物比T的最高价氧化物对应水化物酸性强,所以Z的非金属性大于T,故正确;
故选BD;
故答案为:Cl;BD;
(4)Y的气态氢化物为氨气,X的最高价氧化物对应水化物是碳酸,二者反应生成碳酸铵或碳酸氢铵,碳酸铵或碳酸氢铵都属于离子晶体,故答案为:离子.
点评:本题考查了物质结构和性质、元素周期律等知识点,根据物质的构成微粒、金属性强弱的判断方法等知识点来分析解答,注意铵根离子电子式的书写,为易错点.

练习册系列答案
相关题目
X、Y、Z三种元素位于周期表中同一周期,其最高价氧化物分别为酸性氧化物、碱性氧化物、两性氧化物,则这三种元素原子序数的大小顺序是( )
| A、X>Y>Z |
| B、X>Z>Y |
| C、Y>X>Z |
| D、Y>Z>X |
下列化学反应的离子方程式正确的是( )
| A、澄清石灰水中通入过量二氧化碳Ca2++CO2+2OH-═CaCO3↓+H2O | ||
B、氢氧化钡溶液与稀硫酸反应:Ba2++OH-+H++SO
| ||
| C、氢氧化铜加到稀盐酸中:Cu(OH)2+2H+═Cu2++2H2O | ||
| D、向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+ |
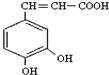 )也叫3,4-二羟基桂皮酸,它存在于许多种药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,对内脏的止血效果较好,毒性较小,还有镇咳、祛痰等疗效.
)也叫3,4-二羟基桂皮酸,它存在于许多种药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,对内脏的止血效果较好,毒性较小,还有镇咳、祛痰等疗效.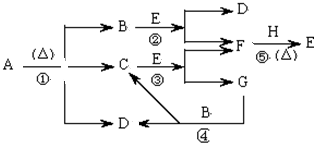

 (系统命名)
(系统命名)