题目内容
关于工业制金刚砂的反应:SiO2+3C
SiC+2CO↑,下列说法中正确的是( )
| ||
| A、SiO2是氧化剂,C为还原剂 |
| B、碳的还原性比硅强 |
| C、氧化剂和还原剂的物质的量之比为2:1 |
| D、1mol SiO2参与反应时,转移电子4mol |
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应中C元素化合价由0价变为-4价、+2价,Si元素和O元素化合价不变,所以C是氧化剂和还原剂,二氧化硅既不是氧化剂也不是还原剂,再结合二氧化硅和转移电子之间的关系式计算.
解答:
解:A.二氧化硅中Si元素和O元素化合价不变,所以二氧化硅既不是氧化剂也不是还原剂,C元素化合价由0价变为-4价、+2价,氧化剂和还原剂都是C,故A错误;
B.碳的非金属性大于Si,所以C的氧化性比Si强,故B错误;
C.氧化剂和还原剂的物质的量之比为1:2,故C错误;
D.1mol SiO2参与反应时,需要1molC作氧化剂,则转移电子的物质的量=1mol×(4-0)=4mol,故D正确;
故选D.
B.碳的非金属性大于Si,所以C的氧化性比Si强,故B错误;
C.氧化剂和还原剂的物质的量之比为1:2,故C错误;
D.1mol SiO2参与反应时,需要1molC作氧化剂,则转移电子的物质的量=1mol×(4-0)=4mol,故D正确;
故选D.
点评:本题考查了氧化还原反应,根据元素化合价变化及基本概念来分析解答,注意C的作用,该反应中生成CO而不是二氧化碳,为易错点.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
下列化学反应能用离子方程式H++OH-═H2O表示的是( )
| A、硫酸氢钠溶液与氢氧化钾溶液反应 |
| B、稀硫酸与氢氧化钡溶液反应 |
| C、稀硝酸与氢氧化铜反应 |
| D、醋酸与氢氧化钠溶液反应 |
下列溶液中,跟100mL 0.15mol/LNa2SO4溶液所含的SO42-物质的量浓度相同的是( )
| A、200 mL 0.15 mol/L MgSO4 溶液 |
| B、50 mL 0.05 mol/L Al2(SO4)3溶液 |
| C、150 mL 1 mol/L Na2SO4 溶液 |
| D、300 mL 0.5 mol/L CuSO4 溶液 |
下列说法正确的是( )
| A、标准状况下,11.2LHCl中含 6.02×1023个离子 |
| B、△H<0,△S>0的化学反应一定能自发进行 |
| C、pH=5的盐酸,稀释1000倍后,溶液pH约为8 |
| D、NaHA溶液PH>7,则c(Na+)=c(HA-)+c(H2A)+2c(A2-) |
下列化学反应的离子方程式正确的是( )
| A、澄清石灰水中通入过量二氧化碳Ca2++CO2+2OH-═CaCO3↓+H2O | ||
B、氢氧化钡溶液与稀硫酸反应:Ba2++OH-+H++SO
| ||
| C、氢氧化铜加到稀盐酸中:Cu(OH)2+2H+═Cu2++2H2O | ||
| D、向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+ |
下列关于Al与Fe的叙述中,一定相等的是( )
| A、Fe分别与盐酸和氯气在一定条件下反应,生成物的价态 |
| B、等质量的Fe分别在空气中氧化或与水蒸气高温反应转移的电子数 |
| C、相同状况,等质量的Al分别与足量盐酸或NaOH溶液反应生成的H2体积 |
| D、等浓度等体积的盐酸和NaOH溶液分别与足量Al反应生成的H2质量 |
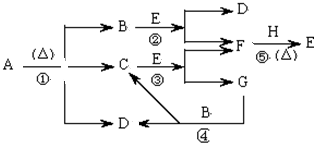
 (系统命名)
(系统命名)