题目内容
1.常温下,下列各组离子在指定的环境中能大量存在的是( )| A. | pH=1的无色溶液中:SO42ˉ、Cu2+、Na+、Clˉ | |
| B. | 中性溶液中:Fe3+、Al3+、NO3ˉ、Clˉ | |
| C. | 能使石蕊试纸变蓝色的溶液中:Na+、K+、S2ˉ、CO32ˉ | |
| D. | 水电离出的c(H+)=1×10ˉ12mol•Lˉ1的溶液中:K+、Na+、Clˉ、HCO3ˉ |
分析 A.铜离子为有色离子;
B.铝离子、铁离子只能存在于酸性溶液中;
C.该溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
D.水电离出的c(H+)=1×10ˉ12mol•Lˉ1的溶液中存在大量氢离子或氢氧根离子,碳酸氢根离子与氢氧根离子反应.
解答 解:A.Cu2+为有色的离子,在溶液中不能大量共存,故A错误;
B.Fe3+、Al3+离子只能存在于酸性溶液中,在中性溶液中不能大量共存,故B错误;
C.能使石蕊试纸变蓝色的溶液中存在大量氢氧根离子,Na+、K+、S2ˉ、CO32ˉ之间不反应,都不与氢氧根离子反应,在溶液中能大量共存,故C正确;
D.水电离出的c(H+)=1×10ˉ12mol•Lˉ1的溶液存在大量氢离子或氢氧根离子,HCO3ˉ与氢氧根离子反应,在碱性溶液中不能大量共存,故D错误;
故选C.
点评 本题考查了离子共存的判断,题目难度中等,明确离子反应发生条件为解答关键,注意熟练掌握离子不能共存的条件,如发生复分解反应、发生氧化还原反应等,还有明确题中暗含条件的要求,如无色溶液中不存在有色离子、酸性溶液中存在大量氢离子等.

练习册系列答案
相关题目
11.下列关于纯净物、混合物、强电解质、弱电解质和非电解质的正确组合是( )
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 漂白粉 | 苏打 | 水 | 氨气 |
| B | 氢氧化钡 | 氢氧化铁胶体 | 硫酸钡 | 氨水 | 乙醇 |
| C | 明矾 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
| D | 石灰石 | 水玻璃 | 氯化钙 | 氢氧化铝 | 碳酸钙 |
| A. | A | B. | B | C. | C | D. | D |
9.在体积恒定的密闭容器中,一定量的SO2与1.25mol O2在催化剂作用下加热到600℃发生反应:2SO2(g)+O2(g) $?_{加热}^{催化剂}$2SO3(g)△H<0.当气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%.下列有关叙述正确的是( )
| A. | 该温度下的平衡常数为101.25 L/moL | |
| B. | 达到平衡时,SO2的转化率是90% | |
| C. | 降低温度,正反应速率减小程度比逆反应速率减小程度大 | |
| D. | 将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为231.4g |
16.有机物M的分子式为C6 H10O4,且1mol M与足量NaHCO3溶液反应会生成2mol气体,则M的结构(不包括立体异构)可能有( )
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
6.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合后所得溶液的pH如表:
请回答:
(1)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2mol•Lˉ1否
(选填“是”或“否”);该混合溶液中离子浓度c(Aˉ)与c(Na+)的大小关系是C;
A.前者大 B.后者大 C.二者相等 D.无法判断
(2)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)=c(A-)=c(OH-)=c(H+);
(3)丁组实验所得混合溶液中,写出下列算式的精确结果(不能做近似计算,回答准确值,结果不一定要化简).c(Na+)-c(Aˉ)=10-5-10-9 mol•Lˉ1.
请回答:
| 实验编号 | HA物质的量浓度(mol•L1) | NaOH物质的量浓度(mol•Lˉ1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | a |
| 乙 | c1 | 0.2 | 7 |
| 丙 | 0.1 | 0.1 | 7 |
| 丁 | 0.1 | 0.1 | 9 |
(选填“是”或“否”);该混合溶液中离子浓度c(Aˉ)与c(Na+)的大小关系是C;
A.前者大 B.后者大 C.二者相等 D.无法判断
(2)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)=c(A-)=c(OH-)=c(H+);
(3)丁组实验所得混合溶液中,写出下列算式的精确结果(不能做近似计算,回答准确值,结果不一定要化简).c(Na+)-c(Aˉ)=10-5-10-9 mol•Lˉ1.
13.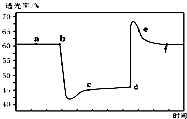 已知反应:2NO2(g)+4CO(g)?N2(g)+4CO2(g)△H<0.将一定量的NO2与CO充入装有催化剂的注射器中后封口.右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法不正确的是( )
已知反应:2NO2(g)+4CO(g)?N2(g)+4CO2(g)△H<0.将一定量的NO2与CO充入装有催化剂的注射器中后封口.右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法不正确的是( )
 已知反应:2NO2(g)+4CO(g)?N2(g)+4CO2(g)△H<0.将一定量的NO2与CO充入装有催化剂的注射器中后封口.右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法不正确的是( )
已知反应:2NO2(g)+4CO(g)?N2(g)+4CO2(g)△H<0.将一定量的NO2与CO充入装有催化剂的注射器中后封口.右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法不正确的是( )| A. | b点的操作是快速压缩注射器 | |
| B. | c点与a点相比,c(NO2)、c(N2)都增大 | |
| C. | e点:υ(正)<υ(逆) | |
| D. | 若考虑体系温度变化,且没有能量损失,则平衡常数K(c)>K(f) |

 .
. .
. .
. ,A与等物质的量的Br2进行加成反应的产物共有3种(不考虑立体异构).
,A与等物质的量的Br2进行加成反应的产物共有3种(不考虑立体异构).