题目内容
10.下列物质之间能够发生如图所示的化学反应,合金由两种金属组成,取C溶液进行焰色反应则火焰呈黄色.在反应中产生的水均未在图中标出.
请回答:
(1)写出下列物质的化学式:A:Na M:Al2O3 H:Fe(OH)3
(2)写出下列反应的化学方程式,并标出电子转移情况:
G→H:

(3)写出下列反应的离子方程式:
A→B+C:2Na+2H2O=2Na++2OH-+H2↑
K→D:Al(OH)3+OH-═AlO2-+2H2O.
分析 框图中的“合金”由两种金属组成,H为红褐色沉淀,G→H的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,则G为Fe(OH)2,H为Fe(OH)3,H加热分解得到I为Fe2O3,根据元素守恒可知,合金中含有Fe,C溶液进行焰色反应,则火焰呈黄色,则含有Na元素,而A与水反应得到C与气体B,故C为NaOH,合金与C溶液反应而分离得到固体E与D溶液,则合金含有Al,可推知E为Fe,F为FeCl2,B为H2,则A为Na,结合转化关系,可知D为NaAlO2,K为Al(OH)3,L为AlCl3,M为Al2O3,据此解答.
解答 解:框图中的“合金”由两种金属组成,H为红褐色沉淀,G→H的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,则G为Fe(OH)2,H为Fe(OH)3,H加热分解得到I为Fe2O3,根据元素守恒可知,合金中含有Fe,C溶液进行焰色反应,则火焰呈黄色,则含有Na元素,而A与水反应得到C与气体B,故C为NaOH,合金与C溶液反应而分离得到固体E与D溶液,则合金含有Al,可推知E为Fe,F为FeCl2,B为H2,则A为Na,结合转化关系,可知D为NaAlO2,K为Al(OH)3,L为AlCl3,M为Al2O3.
(1)由上述分析可知,A为Na,M为Al2O3,H为Fe(OH)3,故答案为:Na;Al2O3;Fe(OH)3;
(2)由上述分析可知,合金的成分为Fe、Al,故答案为:Fe、Al;
(3)G→H的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,标出电子转移情况: ,
,
故答案为: ;
;
(3)A→B+C是钠与水的反应,反应离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,
K→D是氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;Al(OH)3+OH-═AlO2-+2H2O.
点评 本题考查无机物的推断,涉及Al、Fe元素化合物的性质与转化,注意根据物质的颜色、焰色反应结合转化关系推断,题目难度中等.

| A. | pH=1的无色溶液中:SO42ˉ、Cu2+、Na+、Clˉ | |
| B. | 中性溶液中:Fe3+、Al3+、NO3ˉ、Clˉ | |
| C. | 能使石蕊试纸变蓝色的溶液中:Na+、K+、S2ˉ、CO32ˉ | |
| D. | 水电离出的c(H+)=1×10ˉ12mol•Lˉ1的溶液中:K+、Na+、Clˉ、HCO3ˉ |
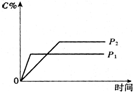 温度一定时,压强分别为P1,P2的条件下,A(g)+2B(g)?nC(g) 的反应体系中,C的分数与时间t,压强P1,P2的关系如图所示,则下列结论正确的是( )
温度一定时,压强分别为P1,P2的条件下,A(g)+2B(g)?nC(g) 的反应体系中,C的分数与时间t,压强P1,P2的关系如图所示,则下列结论正确的是( )| A. | P1>P2,n<3 | B. | P1<P2,n=3 | C. | P1<P2,n>3 | D. | P1>P2,n>3 |
 (1)实验室常用装置E制备Cl2,写出该反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(1)实验室常用装置E制备Cl2,写出该反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.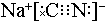 ,碳元素的化合价为+2;用ClO2处理泄漏的氰化钠,得到无毒的NaCl、N2和CO2.若处理4×10-5mol•L-1的废水1000L,至少需要ClO2的质量为2.7g.
,碳元素的化合价为+2;用ClO2处理泄漏的氰化钠,得到无毒的NaCl、N2和CO2.若处理4×10-5mol•L-1的废水1000L,至少需要ClO2的质量为2.7g.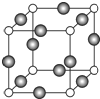 已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期的p区元素且最外层只有2对成对电子,F元素原子序数为29.
已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期的p区元素且最外层只有2对成对电子,F元素原子序数为29.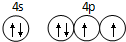 .
.