题目内容
下列说法正确的是( )
| A、△H>0、△S>0的反应一定不能自发进行 |
| B、反应4Al(s)+3O2(g)=2Al2O3 (s)的△H<0、△S>0 |
| C、反应物分子有效碰撞次数增加则反应物的浓度一定增加 |
| D、压强和浓度对反应速率的影响都是通过改变单位体积活化分子数从而影响有效碰撞次数实现的 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、反应自发进行的判断依据△H-T△S<0分析;
B、反应是气体体积减小的反应,熵变减小;
C、升温也可以增加有效碰撞;
D、压强改变浓度改变,浓度改变单位体积活化分子数变化;
B、反应是气体体积减小的反应,熵变减小;
C、升温也可以增加有效碰撞;
D、压强改变浓度改变,浓度改变单位体积活化分子数变化;
解答:
解:A、反应自发进行的判断依据△H-T△S<0分析,△H>0、△S>0的反应,高温下能自发进行,故A错误;
B、反应是气体体积减小的反应,熵变减小、△S<0,故B错误;
C、升温也可以增加有效碰撞,反应物分子有效碰撞次数增加则反应物的浓度不一定增加,故C错误;
D、压强改变浓度改变,浓度改变单位体积活化分子数变化,压强和浓度对反应速率的影响都是通过改变单位体积活化分子数从而影响有效碰撞次数实现的,故D正确;
故选D.
B、反应是气体体积减小的反应,熵变减小、△S<0,故B错误;
C、升温也可以增加有效碰撞,反应物分子有效碰撞次数增加则反应物的浓度不一定增加,故C错误;
D、压强改变浓度改变,浓度改变单位体积活化分子数变化,压强和浓度对反应速率的影响都是通过改变单位体积活化分子数从而影响有效碰撞次数实现的,故D正确;
故选D.
点评:本题考查外界条件对反应速率的影响,题目难度不大,注意浓度、压强、温度以及催化剂对活化分子的影响的不同.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有机物X的组成为CnH2nOm,其蒸气相对氢气的密度为51,X中氧元素的质量分数为31.37%,则X的能在NaOH溶液中发生化学反应的同分异构体(不考虑立体异构)有( )
| A、12种 | B、13种 |
| C、14种 | D、15种 |
近两年来,“雾霾”一直是人们所关注的对象,如图为雾霾的主要成分示意图.下列说法不正确的是( )


| A、大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
| B、重金属离子可导致蛋白质变性 |
| C、SO2和NxOy均属于酸性氧化物 |
| D、苯是最简单的芳香烃 |
 在密闭容器中发生反应:X+3Y═2Z(该反应放热),其中Z呈气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图.下列判断正确的是( )
在密闭容器中发生反应:X+3Y═2Z(该反应放热),其中Z呈气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图.下列判断正确的是( )| A、T1大于T2 |
| B、Y一定呈气态 |
| C、升高温度,该反应的正反应速率减小 |
| D、当n(X):n(Y):n(Z)=1:3:2时,反应一定达到平衡状态 |
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ |
| C、在101kPa时,2g的氢气完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
| D、由C(s,石墨)=C(s,金刚石)△H=+1.90kJ/mol可知,石墨比金刚石稳定 |
下列变化规律错误的是( )
| A、微粒半径:F-<Cl-<Br -<I- |
| B、稳定性:HI<HBr<HCl<HF |
| C、沸点:HF<HCl<HBr<HI |
| D、阴离子还原性:F-<Cl -<Br -<I - |
在一可压缩的密闭容器中,发生可逆反应:M(g)+N(?)P(g)+Q(g)△H>0,当压缩体积时,M的转化率不变.在其它条件不变的情况下,采用以下措施使M的转化率增大( )
| A、加入一定量的M |
| B、加入一定量的不与M、N、P、Q反应的气体 |
| C、反应温度升高 |
| D、加入某物质作催化剂 |
用酸性氢氧燃料电池为电源进行电解的实验装置如图所示.下列说法正确的是( )
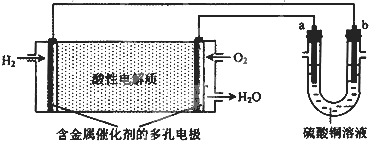

| A、a为负极,b为正极 |
| B、若a极是铁,b极是铜,b极逐渐溶解,a极上有铜析出 |
| C、若a、b极都是石墨,在相同条件下,理论上a极产生的气体与电池中消耗的O2体积相等 |
| D、若电解精炼粗铜时,b极是粗铜,a极是纯铜 |

 有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式
有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式