题目内容
14.在通风橱中进行下列实验:| 步骤 |  |  | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| A. | Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2═2NO2 | |
| B. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| C. | 对此Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
分析 A.硝酸具有强氧化性,与Fe反应生成NO,NO遇空气变为二氧化氮;
B.浓硝酸具有强氧化性,Fe表面形成致密的氧化层,发生钝化现象;
C.对比I、Ⅱ的现象,Fe与稀硝酸反应生成NO,而Fe与浓硝酸反应生成二氧化氮且迅速被钝化,说明浓硝酸的氧化性强于稀硝酸;
D.根据Ⅲ中现象,说明构成原电池,在Fe、Cu之间连接电流计,通过电流计指针偏转,可以判断原电池的正负极.
解答 解:A.稀硝酸具有酸性与强氧化性,与Fe反应生成NO,NO遇空气变为二氧化氮,Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2═2NO2,故A正确;
B.Ⅱ的现象是因为铁发生了钝化,Fe表面形成致密的氧化层,阻止Fe进一步反应,故B正确;
C.对比I、Ⅱ的现象,Fe与稀硝酸反应生成NO,而Fe与浓硝酸反应生成二氧化氮且迅速被钝化,说明浓硝酸的氧化性强于稀硝酸,故C错误;
D.根据Ⅲ中现象,说明构成原电池,在Fe、Cu之间连接电流计,通过电流计指针偏转,可以判断原电池的正负极,进而判断Fe是否被氧化,故D正确,
故选:C.
点评 本题考查硝酸的化学性质、原电池原理,难度不大,侧重考查学生分析解决问题的能力.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
4.在标准状况下,将7g N2、11g CO2和16g SO2混合,该混合气体的体积约是( )
| A. | 5.6L | B. | 11.2L | C. | 16.8L | D. | 22.4L |
5.用O2将HCl转化为Cl2,可提高效益,减少污染.

(1)传统上该转化通过如图1所示的催化循环实现.其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(s)△H1,反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)△H=2(△H1+△H2)(反应热用△H1和△H2表示).
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性.
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的αHCl~T曲线如图2,则总反应的△H<0(填“>”、“=”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是K(A).
②在上述实验中若压缩体积使压强增大,画出相应αHCl~T曲线的示意图,并简要说明理由:增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大.
③下列措施中,有利于提高αHCl的有BD.
A.增大n(HCl) B.增大n(O2)
C.使用更好的催化剂 D.移去H2O
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
计算2.0~6.0min内以HCl的物质的量变化表示的反应速率(以mol•min-1为单位,写出计算过程).
(4)Cl2用途广泛,写出用Cl2制备漂白粉的化学反应方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.

(1)传统上该转化通过如图1所示的催化循环实现.其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(s)△H1,反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)△H=2(△H1+△H2)(反应热用△H1和△H2表示).
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性.
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的αHCl~T曲线如图2,则总反应的△H<0(填“>”、“=”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是K(A).
②在上述实验中若压缩体积使压强增大,画出相应αHCl~T曲线的示意图,并简要说明理由:增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大.
③下列措施中,有利于提高αHCl的有BD.
A.增大n(HCl) B.增大n(O2)
C.使用更好的催化剂 D.移去H2O
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
| t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
(4)Cl2用途广泛,写出用Cl2制备漂白粉的化学反应方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
9.下列有关性质的比较,不能用元素周期律解释的是( )
| A. | 酸性:H2SO4>H3PO4 | B. | 非金属性:Cl>Br | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 热稳定性:Na2CO3>NaHCO3 |
19.下列物质在生话中应用时,起还原作用的是( )
| A. | 明矾作净水剂 | B. | 甘油作护肤保湿剂 | ||
| C. | 漂粉精作消毒剂 | D. | 铁粉作食品袋内的脱氧剂 |
6.中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是( )
| A. | 用胆矾炼铜 | B. | 用铁矿石炼铁 | ||
| C. | 烧结粘土制陶瓷 | D. | 打磨磁石制指南针 |
3.下列说法不正确的是( )
| A. | 液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性 | |
| B. | 常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关 | |
| C. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化 | |
| D. | 燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施 |

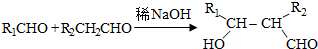
 .
. .
.
 (写结构简式)
(写结构简式)
 .
.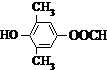 或
或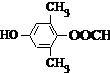 .
.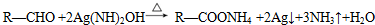 .
.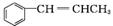 为原料制备
为原料制备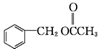 的合成路线流程图如下,试在方框内补充有机物的结构简式:
的合成路线流程图如下,试在方框内补充有机物的结构简式: