题目内容
2.聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容性方面有很好的应用前景. PPG的一种合成路线如下: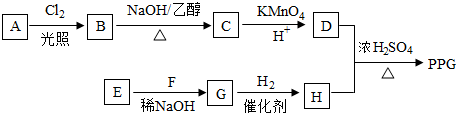
已知:
①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢
②化合物B为单氯代烃:化合物C的分子式为C5H8
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质
④
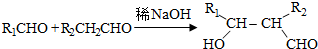
冋答下列问题:
(1)A的结构简式为
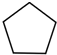 .
.(2)由B生成C的化学方程式为
 .
.(3)由E和F生成G的反应类型为加成反应,G的化学名称为3-羟基丙醛.
(4)①由D和H生成PPG的化学方程式为:
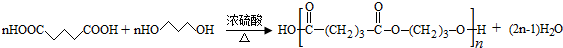
②若PPG平均相对分子质量为10000,则其平均聚合度约为b(填标号).
a. 48b. 58c. 76 d.122
(5)D的同分异构体中能同时满足下列条件的共有5种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体②既能发生银镜反应,又能发生水解反应
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是
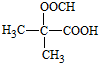 (写结构简式)
(写结构简式)D的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是c(填标号).
a.质谱仪 b.红外光谱仪c.元素分析仪d.核磁共振仪.
分析 烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢,$\frac{70}{12}$=5…10,则A为C5H10,结构为 ;A发生光照下取代反应生成B为
;A发生光照下取代反应生成B为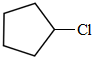 ,B发生消去反应生成C为
,B发生消去反应生成C为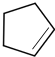 ,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(
,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG( ),以此来解答.
),以此来解答.
解答 解:烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢,$\frac{70}{12}$=5…10,则A为C5H10,结构为 ;A发生光照下取代反应生成B为
;A发生光照下取代反应生成B为 ,B发生消去反应生成C为
,B发生消去反应生成C为 ,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(
,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG( ),
),
(1)A的结构简式为 ,故答案为:
,故答案为: ;
;
(2)由B生成C的化学方程式为 ,
,
故答案为: ;
;
(3)由E和F生成G的反应类型为加成反应,G的化学名称为3-羟基丙醛,故答案为:加成反应;3-羟基丙醛;
(4)①由D和H生成PPG的化学方程式为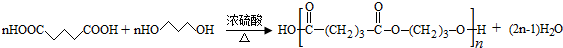 ,
,
故答案为: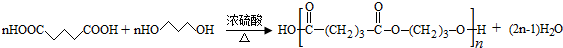 ;
;
②若PPG平均相对分子质量为10000,则其平均聚合度约为$\frac{10000}{12×8+16×4+1×12}$≈58,故答案为:b;
(5)D的同分异构体中能同时满足①能与饱和NaHCO3溶液反应产生气体,含-COOH,②既能发生银镜反应,又能发生水解反应-COOCH,D中共5个C,则含3个C-C-C上的2个H被-COOH、-OOCH取代,共为3+2=5种,含其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是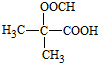 ,D及同分异构体中组成相同,由元素分析仪显示的信号(或数据)完全相同,故答案为:5;
,D及同分异构体中组成相同,由元素分析仪显示的信号(或数据)完全相同,故答案为:5; ;c.
;c.
点评 本题考查有机物的推断,为高频考点,为2015年高考真题,把握合成中碳链变化、官能团变化及反应条件推断物质为解答的关键,侧重分析与推断能力的综合考查,题目难度中等.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案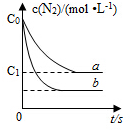 等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),下图曲线a表示该反应在T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )
等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),下图曲线a表示该反应在T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )| A. | T℃时,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$ | |
| B. | T℃时,随着反应的进行,混合气体的密度减小 | |
| C. | 曲线b对应的条件改变可能是加入了催化剂 | |
| D. | 若曲线b对应的条件改变是温度,可判断该反应的△H<0 |
| A. | 60g丙醇中存在的共价键总数为10NA | |
| B. | 1L 0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 钠在空气中燃烧可生成多种氧化物.23g钠充分燃烧时转移电子数为1NA | |
| D. | 235g核素92235U发生裂变反应:92235U+01n$\stackrel{裂变}{→}$3890Sr+54136Xe+1001n净产生的中子(01n)数为10NA |
| 步骤 |  |  | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| A. | Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2═2NO2 | |
| B. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| C. | 对此Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x kJ•mol-1
已知:
碳的燃烧热△H1=a kJ•mol-1
S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1
则x为( )
| A. | 3a+b-c | B. | c-3a-b | C. | a+b-c | D. | c-a-b |
| A. | NaHSO4溶液与Ba(OH)2溶液反应 | B. | C6H5ONa溶液与CO2反应 | ||
| C. | NaAlO2溶液与CO2反应 | D. | Fe与稀硝酸反应 |
 .
. .
.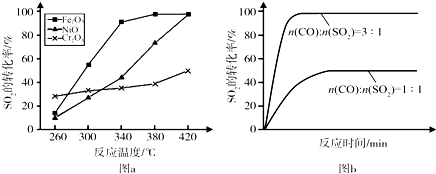
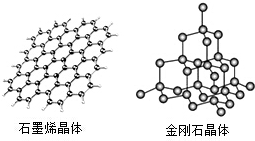 碳及其化合物广泛存在于自然界中,回答下列问题:
碳及其化合物广泛存在于自然界中,回答下列问题: