题目内容
19.下列物质在生话中应用时,起还原作用的是( )| A. | 明矾作净水剂 | B. | 甘油作护肤保湿剂 | ||
| C. | 漂粉精作消毒剂 | D. | 铁粉作食品袋内的脱氧剂 |
分析 物质起还原作用,则该物质作还原剂,其化合价要升高,据此分析.
解答 解:A.明矾净水时铝离子发生水解反应,没有元素化合价的变化,故A错误;
B.甘油作护肤保湿剂,是利用的其物理性质,没有元素化合价的变化,故B错误;
C.漂粉精作消毒剂,氯元素的化合价降低,作氧化剂,故C错误;
D.铁粉作食品袋内的脱氧剂,Fe与氧气反应,铁的化合价升高,作还原剂,起到还原作用,故D正确.
故选D.
点评 本题考查了氧化还原反应,侧重于还原剂的判断的考查,题目难度不大,注意根据化合价的变化分析.

练习册系列答案
相关题目
9.用下列实验装置进行相应实验,能达到实验目的是( )


| A. | 用①分离NaCl溶液和NaOH溶液 | |
| B. | 用②蒸干NH4Cl和饱和溶液获取NH4Cl晶体 | |
| C. | 用③配制100mL 0.1000mol•L-1 K2Cr2O2溶液 | |
| D. | 用④分离Na2CO3溶液和CH3COOC2H5 |
10. 等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),下图曲线a表示该反应在T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )
等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),下图曲线a表示该反应在T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )
 等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),下图曲线a表示该反应在T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )
等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),下图曲线a表示该反应在T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )| A. | T℃时,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$ | |
| B. | T℃时,随着反应的进行,混合气体的密度减小 | |
| C. | 曲线b对应的条件改变可能是加入了催化剂 | |
| D. | 若曲线b对应的条件改变是温度,可判断该反应的△H<0 |
14.在通风橱中进行下列实验:
下列说法不正确的是( )
| 步骤 |  |  | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| A. | Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2═2NO2 | |
| B. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| C. | 对此Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
11.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x kJ•mol-1
已知:
碳的燃烧热△H1=a kJ•mol-1
S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1
则x为( )
S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x kJ•mol-1
已知:
碳的燃烧热△H1=a kJ•mol-1
S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1
则x为( )
| A. | 3a+b-c | B. | c-3a-b | C. | a+b-c | D. | c-a-b |
8.40℃时,在氨-水体系中不断通入CO2,各种离子的变化趋势如图所示.下列说法不正确的是( )
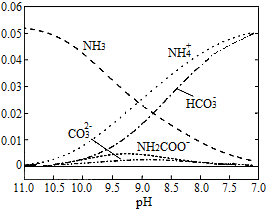

| A. | 在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-) | |
| B. | 不同pH的溶液中存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-) | |
| C. | 随着CO2的通入,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$不断增大 | |
| D. | 在溶液pH不断降低的过程中,有含NH2COO-的中间产物生成 |
6.图示实验能达到实验目的是( )
| A. | 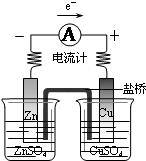 探究原电池原理 探究原电池原理 | B. |  制备无水氯化铁 | C. | 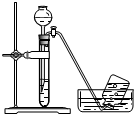 探究铁与水反应 探究铁与水反应 | D. |  收集氨气 收集氨气 |
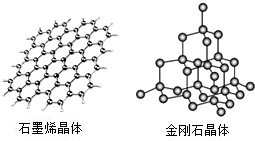 碳及其化合物广泛存在于自然界中,回答下列问题:
碳及其化合物广泛存在于自然界中,回答下列问题: